题目内容
17.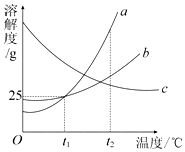 如图为a、b、c三种物质(均不含结晶水)的溶解度曲线,根据图示回答以下问题:
如图为a、b、c三种物质(均不含结晶水)的溶解度曲线,根据图示回答以下问题:(1)t1℃时,物质a和b的溶解度相等;
(2)t1℃时,a物质饱和溶液的质量分数是20%;
(3)将t1℃时接近饱和的a溶液,在不改变其质量分数的情况下,变成饱和溶液,可以采取的方法是降低温度;
(4)将t1℃时a、b、c三种物质的饱和溶液的温度升高到t2℃时,三种溶液的溶质质量分数大小是c>a=b(填写物质序号);
(5)t2℃时,小静向100g水中加入50g a物质,意外发现全部溶解,一段时间后又有部分a物质的晶体析出,你认为“全部溶解”的原因是a物质溶于水放热.
分析 根据溶解度曲线的意义进行分析解答,交点表示两种物质的溶解度相等;根据物质的溶解度随温度的变化特点确定析出晶体的方法,根据饱和溶液的溶质质量分数=$\frac{溶解度}{100g+溶解度}×100%$解答.
解答 解:(1)据图可以看出,在t1℃时,物质a和b的溶解度相等,故填:t1℃;
(2)t1℃时,a的溶解度是25g,故a物质饱和溶液的质量分数是$\frac{25g}{100+25g}×100%$=20%,故填:20%;
(3)将t1℃时接近饱和的a溶液,在不改变其质量分数的情况下,变成饱和溶液,可以采取降低温度的方法,故填:降低温度;
(4)将t1℃时a、b、c三种物质的饱和溶液的温度升高到t2℃时,ab的溶解度随温度的升高而增大,故溶液的组成不变,仍然是t1℃时的溶质质量分数,故ab的溶质质量分数相等,而c的溶解度随温度的升高而减小,会析出晶体,观察图象可以可以看出,在t2℃时c的溶解度大于t1℃时ab的溶解度,故c的溶质质量分数最大,故三种溶液的溶质质量分数大小是c>a=b,故填:c>a=b;
(5)t2℃时,向100g水中加入50g a物质,意外发现全部溶解,一段时间后又有部分a物质的晶体析出,可能是因为a物质溶于放热,温度升高的缘故,故填:a物质溶于水放热.
点评 本题考查了溶解度曲线的意义和应用,完成此题,可以依据已有的知识进行.

练习册系列答案
 天天练口算系列答案
天天练口算系列答案
相关题目
7.我国三峡工程所提供的水电,相当于每年燃烧3000万吨原煤的火力发电厂产生的电能.下列现象中,三峡工程无助于控制的是( )
| A. | 白色污染 | B. | 温室效应 | C. | 酸雨产生 | D. | 粉尘污染 |
5.如图为甲、乙两种物质的溶解度曲线.下列说法正确的是( )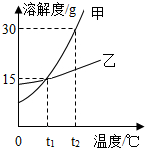

| A. | 甲的溶解度大于乙的溶解度 | |
| B. | t1℃时,甲、乙两种物质的饱和溶液中溶质的质量分数均为15% | |
| C. | 要使接近饱和的乙溶液转化为饱和溶液,可以采用蒸发溶剂的方法 | |
| D. | t2℃时,将50 g甲物质放入100 g水中,得到的溶液的质量为150 g |
7.科学家发现超临界CO2流体是一种具有和水相似、能阻燃、溶解能力强的溶剂,被誉为“绿色环保溶剂”,其密度介于液体和气体之间,下列关于超临界CO2流体说法错误的是( )
| A. | 与干冰的化学性质相同 | B. | 分子间的间隔比CO2气体小 | ||
| C. | 分子不再运动 | D. | 可代替许多有害、有毒、易燃的溶剂 |

 将104g由氯化钠和氯化钡组成的固体混合物溶解于足量的水中,向所得溶液中滴加14.2%的硫酸钠溶液,所加硫酸钠溶液的质量与生成沉淀的质量之间的关系如图所示.
将104g由氯化钠和氯化钡组成的固体混合物溶解于足量的水中,向所得溶液中滴加14.2%的硫酸钠溶液,所加硫酸钠溶液的质量与生成沉淀的质量之间的关系如图所示.