题目内容
取已经在空气中部分变质的氢氧化钠固体样品(样品中的水分忽略不计) 10g,全部溶解在放有50g水的一个大烧杯中,加入64.4g的稀盐酸(盐酸过量),充分反应后称量,烧杯中物质的质量为122.2g.(1)氢氧化钠变质生成了______.
(2)求样品中氢氧化钠的质量分数.
【答案】分析:根据烧碱变质是NaOH与空气中的二氧化碳反应生成碳酸钠和水,碳酸钠能与盐酸反应生辰二氧化碳,根据反应前后物质的质量变化可求出二氧化碳的质量,依据方程式列出比例式,就可计算出样品中碳酸钠的质量,进而计算出样品中氢氧化钠的质量,然后根据质量分数公式计算即可.
解答:解:(1)烧碱变质是NaOH与空气中的二氧化碳反应生成碳酸钠和水;
(2)设样品中碳酸钠的质量为x,
由质量守恒定律可知生成二氧化碳的质量为10g+50g+64.4g-122.2g=2.2g,
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 44
x 2.2g
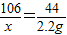
x=5.3g;
样品中氢氧化钠的质量为10g-5.3g=4.7g,
样品中氢氧化钠的质量分数为: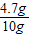 ×100%=47%.
×100%=47%.
答:样品中氢氧化钠的质量分数为47%.
点评:本题考查利用化学方程式进行计算,解题的关键是知道固体氢氧化钠变质的实质以及依据质量守恒定律求出生成的二氧化碳质量.
解答:解:(1)烧碱变质是NaOH与空气中的二氧化碳反应生成碳酸钠和水;
(2)设样品中碳酸钠的质量为x,
由质量守恒定律可知生成二氧化碳的质量为10g+50g+64.4g-122.2g=2.2g,
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 44
x 2.2g
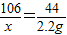
x=5.3g;
样品中氢氧化钠的质量为10g-5.3g=4.7g,
样品中氢氧化钠的质量分数为:
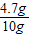 ×100%=47%.
×100%=47%.答:样品中氢氧化钠的质量分数为47%.
点评:本题考查利用化学方程式进行计算,解题的关键是知道固体氢氧化钠变质的实质以及依据质量守恒定律求出生成的二氧化碳质量.

练习册系列答案
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案
相关题目
 25、某兴趣小组对氢氧化钠固体暴露在空气中的变质情况进行了研究.把一小块固体氢氧化钠放在表面皿里,长时间暴露在空气中,发现其固体表面逐渐湿润,部分溶化成液体后又逐渐形成晶体,最终变成粉末.请回答兴趣小组产生的下列问题:
25、某兴趣小组对氢氧化钠固体暴露在空气中的变质情况进行了研究.把一小块固体氢氧化钠放在表面皿里,长时间暴露在空气中,发现其固体表面逐渐湿润,部分溶化成液体后又逐渐形成晶体,最终变成粉末.请回答兴趣小组产生的下列问题: