题目内容
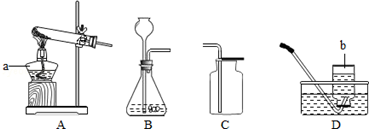
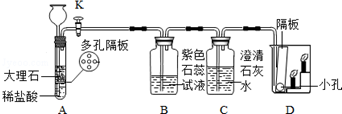
根据下列制取氧气的装置图回答问题.
(1)写出仪器①、②的名称:①
(2)实验室常用高锰酸钾或过氧化氢和二氧化锰来制取氧气,你认为两个方法中相对较好的是
(3)若用A装置制氧气时,a中放
(5)仪器①在滴加液体时,仪器①上的玻璃塞应
(6)小明做实验中手碰到A装置锥形瓶的外壁感到
(7)小明做氧气性质实验时发现铁丝在氧气中没有火星四射,其原因是
(8)小明通过改进实验,做铁丝在氧气中燃烧实验成功了,然后立即用带火星的木条伸进刚做过铁丝燃烧实验的集气瓶中,会出现
分析:(1)如图所示制取氧气的装置,写出常用仪器;
(2)比较用高锰酸钾或过氧化氢和二氧化锰来制取氧气的区别和联系.
(3)①用A装置制氧气时,没有加热装置,所以是过氧化氢和二氧化锰来制取氧气;②制取气体前都要检查装置的气密性,并且要注意其方法;
(4)不旋紧双孔胶塞,产生的气体会逸出,所以导管口没出现气泡.
(5)仪器①在滴加液体时,锥形瓶中过氧化氢和二氧化锰反应产生氧气,并且放热,所以产生大量气泡和白雾;滴加液体速率过快,产生氧气太快,所以反应混合液通过导管进入水槽.
(6)过氧化氢和二氧化锰来制取氧气的反应为放热反应.
(7)铁丝在氧气中没有火星四射,原因有多种:如①未除去铁丝表面的铁锈②收集的氧气纯度不够.
(8)刚做过铁丝燃烧实验的集气瓶中,残留氧气浓度比空气含氧气浓度大,所以带火星的木条复燃.
(2)比较用高锰酸钾或过氧化氢和二氧化锰来制取氧气的区别和联系.
(3)①用A装置制氧气时,没有加热装置,所以是过氧化氢和二氧化锰来制取氧气;②制取气体前都要检查装置的气密性,并且要注意其方法;
(4)不旋紧双孔胶塞,产生的气体会逸出,所以导管口没出现气泡.
(5)仪器①在滴加液体时,锥形瓶中过氧化氢和二氧化锰反应产生氧气,并且放热,所以产生大量气泡和白雾;滴加液体速率过快,产生氧气太快,所以反应混合液通过导管进入水槽.
(6)过氧化氢和二氧化锰来制取氧气的反应为放热反应.
(7)铁丝在氧气中没有火星四射,原因有多种:如①未除去铁丝表面的铁锈②收集的氧气纯度不够.
(8)刚做过铁丝燃烧实验的集气瓶中,残留氧气浓度比空气含氧气浓度大,所以带火星的木条复燃.
解答:解:根据以上分析,知“过氧化氢和二氧化锰反应产生氧气”的装置,氧气的收集,实验的注意事项.
(1)依据实验室常用仪器的认识解决.答案为:分液漏斗;水槽.
(2)用高锰酸钾或过氧化氢和二氧化锰来制取氧气的区别:是否需要加热.
(3)过氧化氢和二氧化锰来制取氧气:不需加热;制取气体前都要检查装置的气密性
(4)旋紧双孔胶塞,防止产生的气体会逸出.
(5)过氧化氢和二氧化锰反应产生氧气,并且放热,所以产生大量气泡和白雾;滴加液体速率过快,产生氧气太快,所以反应混合液通过导管进入水槽.
(6)过氧化氢和二氧化锰来制取氧气的反应为放热反应,所以手碰到A装置锥形瓶的外壁感到发烫.
(7)铁丝在氧气中没有火星四射,原因有多种:如①未除去铁丝表面的铁锈②收集的氧气纯度不够.
(8)刚做过铁丝燃烧实验的集气瓶中,残留氧气浓度比空气含氧气浓度大.
故答为:(1)分液漏斗;水槽 (2)用过氧化氢和二氧化锰制氧气;①不需要加热②可以控制反应的速率③生成物对环境没有污染(任答一个即可) (3)过氧化氢(或H2O2); 二氧化锰(或MnO2); 2H2O2
2H2O+O2↑; 后; 先用止水夹夹紧橡皮管(或关闭导管活塞),再往分液漏斗中注入一定量的水,打开分液漏斗活塞,一段时间后,漏斗内水不能进入锥形瓶,则装置气密性良好. (4)旋紧双孔胶塞 (5)拿掉;产生大量气泡和白雾;反应混合液通过导管进入水槽(其它合理答案也可). (6)发烫;放热反应 (7)①未除去铁丝表面的铁锈②收集的氧气纯度不够③未待火柴将近烧尽时伸入集气瓶中,瓶中氧气被火柴消耗. (8)带火星的木条复燃;集气瓶残留氧气浓度比空气含氧气浓度大
(1)依据实验室常用仪器的认识解决.答案为:分液漏斗;水槽.
(2)用高锰酸钾或过氧化氢和二氧化锰来制取氧气的区别:是否需要加热.
(3)过氧化氢和二氧化锰来制取氧气:不需加热;制取气体前都要检查装置的气密性
(4)旋紧双孔胶塞,防止产生的气体会逸出.
(5)过氧化氢和二氧化锰反应产生氧气,并且放热,所以产生大量气泡和白雾;滴加液体速率过快,产生氧气太快,所以反应混合液通过导管进入水槽.
(6)过氧化氢和二氧化锰来制取氧气的反应为放热反应,所以手碰到A装置锥形瓶的外壁感到发烫.
(7)铁丝在氧气中没有火星四射,原因有多种:如①未除去铁丝表面的铁锈②收集的氧气纯度不够.
(8)刚做过铁丝燃烧实验的集气瓶中,残留氧气浓度比空气含氧气浓度大.
故答为:(1)分液漏斗;水槽 (2)用过氧化氢和二氧化锰制氧气;①不需要加热②可以控制反应的速率③生成物对环境没有污染(任答一个即可) (3)过氧化氢(或H2O2); 二氧化锰(或MnO2); 2H2O2
| ||
点评:(1)此题考查了同学们对常用化学仪器的了解和识记情况,只有很好的认识它们,做实验才能得心应手.(2)重点考查“过氧化氢和二氧化锰反应产生氧气”的装置及注意事项.

练习册系列答案
 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目


 过碳酸钠固体是过氧化氢和碳酸钠加合而成的化合物.其化学式为2Na2CO3?3H2O2,有关该化合物叙述如下.
过碳酸钠固体是过氧化氢和碳酸钠加合而成的化合物.其化学式为2Na2CO3?3H2O2,有关该化合物叙述如下.