题目内容
| |||||||||||||||
答案:1.有气泡冒出;块状碳酸钙逐渐变小,最后全部消失(或溶解);2.HCl,④②③①;3.更换滤纸,重新过滤;
解析:
解析:
|
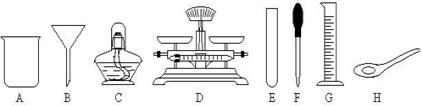
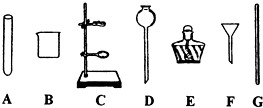
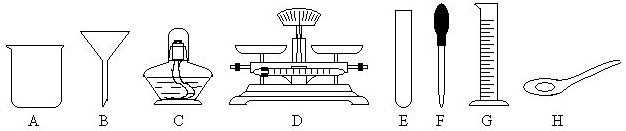
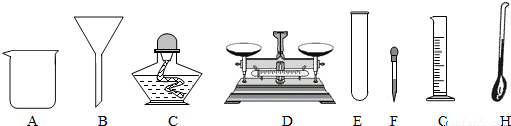
如何从反应液中提取氯化钙晶体.本题考查物质提纯与分离,其基本步骤为:①转化,根据混合物成分及不增加新杂质的除杂原则选择合适的试剂及实验方法将杂质转化.②分离,根据被提纯物及杂质转化后的状态选择分离方法.③检查,根据反应逐一检查被提纯物是否带入新物质并进行处理,如过滤液不澄清,还须更换滤纸,重新过滤. 解答本题关键是确定反应液中溶质的成分:CaCl2、MgCl3、HCl,然后再确定如何将MgCl2、HCl转化为CaCl2,因此加入足量CaO,发生的反应有:CaO+2HCl=CaCl2+H2O、CaO+H2O=Ca(OH)2,溶液中Ca(OH)2+MgCl2=Mg(OH)2↓+CaCl2,然后通过过滤分离出不溶的Ca(OH)2和Mg(OH)2,由于Ca(OH)2微溶,滤液中还含有少量的Ca(OH)2,故加入适量的盐酸进行中和:Ca(OH)2+2HCl=CaCl2+2H2O,最后得到纯净的氯化钙溶液,然后进行蒸发结晶. |

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目