题目内容
11.如图为A、B两物质的溶解度曲线,下列说法正确的是( )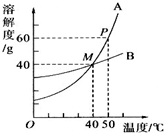
| A. | 40℃时,A、B两物质的溶解度相同 | |
| B. | 50℃时,A物质的饱和溶液溶质质量分数为60% | |
| C. | 降低温度,A、B两物质的溶液均有晶体析出 | |
| D. | B物质中混有少量A物质,可用冷却热饱和溶液的方法提纯 |
分析 根据固体物质的溶解度曲线可以:①比较不同物质在同一温度下的溶解度的大小,②查出某物质在某一温度下的溶解度,从而确定其饱和溶液中溶质的质量分数,饱和溶液中溶质的质量分数=$\frac{溶解度}{100g+溶解度}$×100%,③判断出物质的溶解度随温度变化的变化情况.
解答 解:A、在40℃时,两物质的溶解度曲线交于一点,说明两物质的溶解度相等,且是40g,故正确;
B、50℃时,A的溶解度是60g,则其饱和溶液中溶质的质量分数为:$\frac{60g}{100g+60g}$×100%=37.5%,故错误;
C、由两物质的溶解度曲线不难看出,AB的溶解度随温度的升高而增大,A、B两物质的饱和溶液均有晶体析出,不是饱和溶液不一定析出,故错误;
D、B物质的溶解度受温度影响较小,B中混有少量A物质,可用蒸发溶剂的方法提纯B,故错误.
答案:A.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,从而加深学生对固体溶解度的理解和应用.

练习册系列答案
相关题目
2.下列实验现象的描述,正确的是( )
| A. | 木炭在氧气中燃烧比在空气中燃烧旺,发出白光,并放出热量 | |
| B. | 铁丝在氧气中燃烧,火星四射,生成一种白色固体 | |
| C. | 把盛有红磷的燃烧匙伸人盛氧气的集气瓶中,产生大量白烟 | |
| D. | 硫在空气中燃烧产生淡蓝色火焰,生成二氧化硫气体 |
19.将下列物质取少量分别放入适量水中充分搅拌,能形成溶液的是( )
| A. | 植物油 | B. | 冰块 | C. | 面粉 | D. | 食盐 |
16.某水溶液中含有以下离子中的若干种:K+、Cl-、Ca2+、Zn2+、SO42-、CO32-,现取两份100mL溶液进行如下实验
(1)第一份加入AgNO3溶液有沉淀产生.
(2)第二份加足量BaCl2溶液后,得沉淀物6.63g,经足量硝酸洗涤、干燥后,沉淀质量为4.66g,在所得滤液中加入AgNO3溶液有沉淀产生.根据上述实验,以下推测不正确的是( )
(1)第一份加入AgNO3溶液有沉淀产生.
(2)第二份加足量BaCl2溶液后,得沉淀物6.63g,经足量硝酸洗涤、干燥后,沉淀质量为4.66g,在所得滤液中加入AgNO3溶液有沉淀产生.根据上述实验,以下推测不正确的是( )
| A. | Cl-一定存在 | |
| B. | SO42-、和CO32-一定存在,且二者的个数比为1:2 | |
| C. | Ca2+和Zn2+一定存在 | |
| D. | 100ml溶液中K+的质量不小于2.34g |
20.学校化学兴趣小组的同学知道二氧化锰能作过氧化氢(H2O2)分解的催化剂后,想再探究其他一些物质如氧化铝(Al2O3)是否也可作过氧化氢分解的催化剂.请你一起参与他们的探究过程,并填写下列空白.
【提出问题】Al2O3能不能作过氧化氢分解的催化剂呢?
【作出猜想】Al2O3能作过氧化氢分解的催化剂.
【实验验证】
【得出结论】Al2O3能加快过氧化氢的分解速率,故Al2O3能作过氧化氢分解的催化剂.
在该兴趣小组的同学设计的实验中,“实验一”起对比 作用.
【反思提高】经过讨论,有的同学认为只有上述两个证据,不能证明Al2O3能作过氧化氢分解的催化剂,还要补充一个探究实验三:
实验三:
[实验步骤]①准确称量Al2O3(少量,不溶于水)的质量;②完成实验二;③待反应结束,将实验二试管里的物质进行过滤,洗涤,干燥,称量;④对比反应前后Al2O3的质量.[交流讨论]如果Al2O3在反应前后质量不变,则说明Al2O3可以作过氧化氢分解的催化剂.
提出新的问题】但小华认为,要证明猜想,上述三个实验还不足够,还需要再增加一个探究实验:探究Al2O3在反应前后化学性质不变.
通过补充实验,证明Al2O3能作过氧化氢分解的催化剂,请你写出实验二中发生反应的文字表达式过氧化氢$\stackrel{氧化铝}{→}$水+氧气.
【提出问题】Al2O3能不能作过氧化氢分解的催化剂呢?
【作出猜想】Al2O3能作过氧化氢分解的催化剂.
【实验验证】
| 实验步骤 | 实验现象 | 实验结论 | |
| 实验一 | 将带火星的木条伸入装有过氧化氢溶液的试管中 | 有少量气泡产生;木条不复燃 | 常温下过氧化氢溶液分解速率很慢. |
| 实验二 | 在装有过氧化氢溶液的试管中加入少量Al2O3,然后将带火星的木条伸入试管中 | 有大量气泡产生;木条复燃 | 加入Al2O3,能加快过氧化氢溶液的分解速率 |
在该兴趣小组的同学设计的实验中,“实验一”起对比 作用.
【反思提高】经过讨论,有的同学认为只有上述两个证据,不能证明Al2O3能作过氧化氢分解的催化剂,还要补充一个探究实验三:
实验三:
[实验步骤]①准确称量Al2O3(少量,不溶于水)的质量;②完成实验二;③待反应结束,将实验二试管里的物质进行过滤,洗涤,干燥,称量;④对比反应前后Al2O3的质量.[交流讨论]如果Al2O3在反应前后质量不变,则说明Al2O3可以作过氧化氢分解的催化剂.
提出新的问题】但小华认为,要证明猜想,上述三个实验还不足够,还需要再增加一个探究实验:探究Al2O3在反应前后化学性质不变.
通过补充实验,证明Al2O3能作过氧化氢分解的催化剂,请你写出实验二中发生反应的文字表达式过氧化氢$\stackrel{氧化铝}{→}$水+氧气.
1.下列物质中,属于氧化物的是( )
| A. | 食用醋 | B. | 氧化镁 | C. | 冰红茶 | D. | 加碘盐 |