题目内容
(2010?常州)16g Fe2O3与184g稀H2SO4恰好完全反应,求所得Fe2(SO4)3溶液的溶质质量分数?
【答案】分析:首先根据反应物,生成物和反应条件正确书写方程式,再根据方程式中Fe2O3和Fe2(SO4)3的质量比求出
Fe2(SO4)3的质量,由公式溶液的溶质质量分数= ×100%就可以求出所得Fe2(SO4)3溶液的溶质质量分数.
×100%就可以求出所得Fe2(SO4)3溶液的溶质质量分数.
解答:解:设反应生成的Fe2(SO4)3的质量为x
Fe2O3 ;;+3H2SO4 ;;═Fe2(SO4)3+3H2O
160 400
16g x
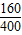 =
=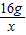
x=40g
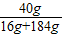 ×100%=20%
×100%=20%
答:所得Fe2(SO4)3溶液的溶质质量分数为20%.
点评:与方程式有关的溶质质量分数的计算经常出现在考题中,大家需仔细分析,认真计算.
Fe2(SO4)3的质量,由公式溶液的溶质质量分数=
 ×100%就可以求出所得Fe2(SO4)3溶液的溶质质量分数.
×100%就可以求出所得Fe2(SO4)3溶液的溶质质量分数.解答:解:设反应生成的Fe2(SO4)3的质量为x
Fe2O3 ;;+3H2SO4 ;;═Fe2(SO4)3+3H2O
160 400
16g x
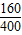 =
=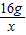
x=40g
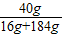 ×100%=20%
×100%=20%答:所得Fe2(SO4)3溶液的溶质质量分数为20%.
点评:与方程式有关的溶质质量分数的计算经常出现在考题中,大家需仔细分析,认真计算.

练习册系列答案
相关题目
(2010?常州二模)碳酸钡广泛应用于显像管(CRT)、陶瓷、光学玻璃等行业.现有碳酸盐矿石(主要成分是BaCO3和CaCO3),以下是从该矿石中分离出BaCO3的流程图.(已知:钡元素化合物的化学性质与钙元素化合物的化学性质相近.)

试回答下列问题:
(1)已知不同温度下Ca(OH)2和Ba(OH)2的溶解度如表:
步骤③加热悬浊液,过滤热溶液的原因是______;
(2)现在25℃时,将10g氢氧化钡放入50g水中,充分搅拌,所得溶液的溶质质量分数为______.(结果保留一位小数)
(3)步骤①中产生的气体是______;步骤④中发生化学反应的方程式为______.
(4)绿色化学又称环境友好化学,其核心是利用化学原理来减少和消除工业生产对环境的影响.上述流程中体现绿色化学理念的是:______.

试回答下列问题:
(1)已知不同温度下Ca(OH)2和Ba(OH)2的溶解度如表:
| 温度(℃) | 0 | 20 | 25 | 60 |
| Ba(OH)2溶解度 | 1.67 | 3.89 | 5.60 | 20.94 |
| Ca(OH)2溶解度 | 0.189 | 0.173 | 0.148 | 0.121 |
(2)现在25℃时,将10g氢氧化钡放入50g水中,充分搅拌,所得溶液的溶质质量分数为______.(结果保留一位小数)
(3)步骤①中产生的气体是______;步骤④中发生化学反应的方程式为______.
(4)绿色化学又称环境友好化学,其核心是利用化学原理来减少和消除工业生产对环境的影响.上述流程中体现绿色化学理念的是:______.
 (2010?常州)如图是某锌锰干电池的剖面图:
(2010?常州)如图是某锌锰干电池的剖面图:
