题目内容
7.将5gA、1gB和2gC置于一密闭容器内加热,反应后分析得知,混合物中除含2gA、4.2gC外,还有一种物质D.已知A、B、C、D的相对分子质量依次是30、20、44、18.求上述反应的化学方程式的表示式.分析 在化学反应中,反应物的质量是减小的,生成物的质量是增大的,判断出反应物和生成物,求出此反应中各物质的质量关系,再根据质量守恒定律,和所给物质的相对分子质量,代入选项中,判断出正确选项.
解答 解:由题意知,A和B反应后质量减小,A和B是反应物,C质量增加,C是生成物,并且生成了新物质D,A减少了5克-2克=3克,B减少了1克,则参加反应的A和B的质量分别为3克和1克,C增加了4.2克-2克=2.2克,则生成了C2.2克,生成D的质量为1克+1克-2.2克=1.8克,从而可以求出四种物质的质量比为:15:5:11:9,A、B、C、D化学计量数之比为:$\frac{15}{30}:\frac{5}{20}:\frac{11}{44}:\frac{9}{18}$=2:1:1:2,化学方程式为:2A+B=C+2D.
故答案为•:2A+B=C+2D.
点评 做对本题的关键是要知道根据方程式找各物质的质量关系时相对分子质量要乘以化学计量数.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10. 按照如图装置,瓶内盛放下列何种物质时灯泡能发光( )
按照如图装置,瓶内盛放下列何种物质时灯泡能发光( )
 按照如图装置,瓶内盛放下列何种物质时灯泡能发光( )
按照如图装置,瓶内盛放下列何种物质时灯泡能发光( )| A. | 蒸馏水 | B. | 蔗糖水 | C. | 食盐固体 | D. | 硫酸钠溶液 |
11.下列实验操作正确的是( )
| A. |  甲烷验纯 | B. |  过滤 | C. |  加热液体 | D. |  稀释浓硫酸 |
8.实验室用锌和稀硫酸制取氢气,下列操作错误的是( )
| A. |  稀释浓硫酸 | B. |  加入锌粒 | C. |  产生氢气 | D. | 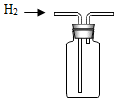 收集氢气 |
2.根据化学方程式H2SO4+Na2SO3═Na2SO4+X+H2O,可推断X的化学式为( )
| A. | SO2 | B. | SO3 | C. | H2S | D. | Na2O |
19.某物质能在氧气中燃烧,却不能在空气中燃烧,是因为( )
| A. | 空气中含有水蒸气 | |
| B. | 空气中含有大量不支持燃烧的二氧化碳 | |
| C. | 空气中含氧气量少 | |
| D. | 空气散热快,温度难达到其着火点 |
16.下列物质,不能由金属单质和盐酸直接反应生成的是( )
| A. | MgCl2 | B. | ZnCl2 | C. | AlCl3 | D. | FeCl3 |
17.下列叙述符合质量守恒定律的是( )
| A. | 气割时,铁板质量一定等于切割后两块铁板和铁渣的质量总和 | |
| B. | 镁条燃烧后固体质量增加,不符合质量守恒定律 | |
| C. | 10 g高锰酸钾完全分解所得生成物的质量总和一定是10 g | |
| D. | 铁丝在氧气中燃烧后增加的质量一定等于集气瓶中氧气的质量 |