题目内容
6.将ag20%的NaOH溶液与ag20%的盐酸溶液混合,滴入紫色石蕊试液后颜色为( )| A. | 紫色 | B. | 蓝色 | C. | 红色 | D. | 无色 |
分析 根据氢氧化钠与盐酸反应的化学方程式,判断完全反应后剩余的是哪一种溶液,再根据紫色石蕊试液遇酸变红色,遇碱变蓝色,遇中性溶液不变色,进行分析判断.
解答 解:将ag20%的NaOH溶液与ag20%的盐酸溶液混合,盐酸与氢氧化钠溶液中所含溶质的质量相等.
反应中消耗盐酸酸与氢氧化钠的质量比关系如下:
HCl+NaOH═NaCl+H2O
36.5 40
可知,36.5份质量的盐酸与40份质量的氢氧化钠恰好完全反应,则将ag20%的NaOH溶液与ag20%的盐酸溶液混合,稀盐酸有剩余,溶液显酸性,最终混合后的液体呈红色.
故选:C.
点评 本题难度不大,掌握中和反应应用,根据化学方程式的计算判断出反应后剩余的物质是正确解答本题的关键.

练习册系列答案
相关题目
14.如图是甲、乙、丙三物质的溶解度曲线,下列说法中正确的是( )


| A. | P点表示甲、丙两种物质的饱和溶液中含溶质质量相等 | |
| B. | t1℃时,乙物质的饱和溶液,升温至t2℃时仍是饱和溶液 | |
| C. | t1℃时,甲物质的饱和溶液中溶质和溶剂的质量比为1:4 | |
| D. | 将甲、乙的饱和溶液分别从t2℃降至t1℃,甲析出晶体较多 |
1.下列各组物间的转化,在一定条件下均能一步实现的一组是( )
| A. | Fe→Fe2O3→FeCl2 | B. | CaCO3→CO2→CO | ||
| C. | CuO→Cu (OH)2→CuSO4 | D. | HNO3→NaNO3→NaCl |
3.下列化学反应与反应类型对应不正确的是( )
| A. | 2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2化合反应 | |
| B. | C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O分解反应 | |
| C. | 2CuO+C$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑置换反应 | |
| D. | AgNO3+HCl═AgCl↓+HNO3置换反应 |
7. 2016年11月21日下午,中科院院士翟婉明院士宣布:世界首条新能源空铁试验线在成都成功投入运行.新能源空铁是指以锂电池为动力源的空中悬挂式轨道列车系统.以下有关说法不正确的是( )
2016年11月21日下午,中科院院士翟婉明院士宣布:世界首条新能源空铁试验线在成都成功投入运行.新能源空铁是指以锂电池为动力源的空中悬挂式轨道列车系统.以下有关说法不正确的是( )
 2016年11月21日下午,中科院院士翟婉明院士宣布:世界首条新能源空铁试验线在成都成功投入运行.新能源空铁是指以锂电池为动力源的空中悬挂式轨道列车系统.以下有关说法不正确的是( )
2016年11月21日下午,中科院院士翟婉明院士宣布:世界首条新能源空铁试验线在成都成功投入运行.新能源空铁是指以锂电池为动力源的空中悬挂式轨道列车系统.以下有关说法不正确的是( )| A. | 空铁的运行将减少空气中二氧化硫、二氧化碳、烟尘等污染物的产生 | |
| B. | 空铁内部有许多铜制导线,铜元素属于金属元素 | |
| C. | 新能源空铁对于缓解交通拥堵,方便公众出行具有重大意义 | |
| D. | 该新型轨道交通系统采用新能源、新材料、新设计,集成若干相关成熟技术建造 |
8.日常生活中下列物质能使紫色石蕊试液变红的是( )
| A. | 蒸馏水 | B. | 食盐水 | C. | 食醋 | D. | 石灰水 |
 如图是甲、乙两种固体的溶解度曲线,t2℃时,45g甲和10g乙完全溶解于100g蒸馏水,冷却到t1℃后,没有(“有”或“没有”)乙析出,有15g甲结晶析出,把t1℃时溶有75g甲的饱和溶液稀释为20%,需加水11.5g.
如图是甲、乙两种固体的溶解度曲线,t2℃时,45g甲和10g乙完全溶解于100g蒸馏水,冷却到t1℃后,没有(“有”或“没有”)乙析出,有15g甲结晶析出,把t1℃时溶有75g甲的饱和溶液稀释为20%,需加水11.5g.
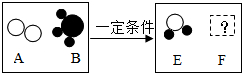
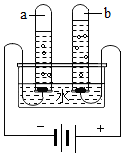 水是人及一切生物生存所必需的,为了人类和社会经济的可持续发展,我们应该了解有关水的一些知识.请你回答:
水是人及一切生物生存所必需的,为了人类和社会经济的可持续发展,我们应该了解有关水的一些知识.请你回答: