题目内容
 钙是维持人体正常功能所必需的元素,如图为某种补钙剂“钙尔奇”说明书的一部分,取1片钙尔奇放入盛有10g稀盐酸的烧杯中,其中的碳酸钙跟盐酸恰好完全反应(其他成分不与盐酸反应),烧杯内物质的质量为11.34g,试计算:
钙是维持人体正常功能所必需的元素,如图为某种补钙剂“钙尔奇”说明书的一部分,取1片钙尔奇放入盛有10g稀盐酸的烧杯中,其中的碳酸钙跟盐酸恰好完全反应(其他成分不与盐酸反应),烧杯内物质的质量为11.34g,试计算:
(1)每片钙尔奇中含碳酸钙的质量为______.
(2)服用这种补钙剂,每人每天摄入钙元素的质量为______.
(3)所用稀盐酸的溶质质量分数是多少?
解:(1)设每片钙尔奇中CaCO3的质量为x,10g盐酸中HCl的质量为y.
完全反应后产生的二氧化碳的质量为:2g+10g-11.34g=0.66g
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 73 44
x y 0.66g
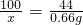
x=1.5g

y=1.095g
(2)碳酸钙中钙元素的质量分数为: ×100%=40%
×100%=40%
每天摄入的钙尔奇中钙元素的质量为:1.5g×2×40%=1.2g.
(3)所用盐酸中HCl的质量分数为: ×100%=10.95%.
×100%=10.95%.
答:(1)每片钙尔奇中含碳酸钙的质量为1.5g;(2)使用这种补钙剂,每人每天摄入钙元素的质量为1.2g;(3)所用稀盐酸中溶质的质量分数为10.95%.
分析:(1)欲正确解答本题,须根据盐酸与碳酸钙反应的化学方程式,得出各物质之间的质量比,列出比例式,即可求出每片钙尔奇中含碳酸钙的质量;
(2)欲正确解答本题,须先根据元素的质量分数公式计算出碳酸钙中钙元素的质量分数,由说明书可知,使用这种补钙剂,每人每天需服用2片,则每人每天摄入钙元素的质量=每片钙尔奇中CaCO3的质量×2片×碳酸钙中钙元素的质量分数,据此答题.
(3)由(1)已计算出10g盐酸中HCl的质量,根据溶质质量分数=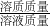 ×100%即可计算出所用盐酸中HCl的质量分数.
×100%即可计算出所用盐酸中HCl的质量分数.
点评:本题主要考查学生运用化学方程式和溶质质量分数公式进行计算的能力.学生需认真分析已知条件中的数量关系,正确书写化学方程式,才能解答.
完全反应后产生的二氧化碳的质量为:2g+10g-11.34g=0.66g
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 73 44
x y 0.66g
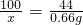
x=1.5g

y=1.095g
(2)碳酸钙中钙元素的质量分数为:
 ×100%=40%
×100%=40%每天摄入的钙尔奇中钙元素的质量为:1.5g×2×40%=1.2g.
(3)所用盐酸中HCl的质量分数为:
 ×100%=10.95%.
×100%=10.95%.答:(1)每片钙尔奇中含碳酸钙的质量为1.5g;(2)使用这种补钙剂,每人每天摄入钙元素的质量为1.2g;(3)所用稀盐酸中溶质的质量分数为10.95%.
分析:(1)欲正确解答本题,须根据盐酸与碳酸钙反应的化学方程式,得出各物质之间的质量比,列出比例式,即可求出每片钙尔奇中含碳酸钙的质量;
(2)欲正确解答本题,须先根据元素的质量分数公式计算出碳酸钙中钙元素的质量分数,由说明书可知,使用这种补钙剂,每人每天需服用2片,则每人每天摄入钙元素的质量=每片钙尔奇中CaCO3的质量×2片×碳酸钙中钙元素的质量分数,据此答题.
(3)由(1)已计算出10g盐酸中HCl的质量,根据溶质质量分数=
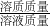 ×100%即可计算出所用盐酸中HCl的质量分数.
×100%即可计算出所用盐酸中HCl的质量分数.点评:本题主要考查学生运用化学方程式和溶质质量分数公式进行计算的能力.学生需认真分析已知条件中的数量关系,正确书写化学方程式,才能解答.

练习册系列答案
相关题目
 钙是维持人体正常功能所必需的元素.右图所示为某种补钙剂“钙尔奇”说明书的一部分.取1片钙尔奇,放入盛有10g稀盐酸的烧杯中,其中碳酸钙跟盐酸恰好完全反应(其它成分与盐酸不反应).烧杯内物质质量变为11.34g.试计算:
钙是维持人体正常功能所必需的元素.右图所示为某种补钙剂“钙尔奇”说明书的一部分.取1片钙尔奇,放入盛有10g稀盐酸的烧杯中,其中碳酸钙跟盐酸恰好完全反应(其它成分与盐酸不反应).烧杯内物质质量变为11.34g.试计算: 钙是维持人体正常功能所必需的元素.右图所示为某种补钙剂“钙尔奇”说明书的一部分.试进行有关的计算:
钙是维持人体正常功能所必需的元素.右图所示为某种补钙剂“钙尔奇”说明书的一部分.试进行有关的计算: (2009?邵阳)钙是维持人体正常功能所必需的元素.小芳服用的某种钙片的部分说明如图1,她很想知道每天服用的钙片中碳酸钙的质量.于是在家中进行了探究:取2片钙片,放人玻璃杯中,向其中加入60g 白醋,两者恰好完全反应(假设钙片中其他成分不与醋酸反应),测得玻璃杯中物质的质量(m)与反应时间(t)的关系如图2所示.反应的化学方程式:
(2009?邵阳)钙是维持人体正常功能所必需的元素.小芳服用的某种钙片的部分说明如图1,她很想知道每天服用的钙片中碳酸钙的质量.于是在家中进行了探究:取2片钙片,放人玻璃杯中,向其中加入60g 白醋,两者恰好完全反应(假设钙片中其他成分不与醋酸反应),测得玻璃杯中物质的质量(m)与反应时间(t)的关系如图2所示.反应的化学方程式: 钙是维持人体正常功能所必需的元素.图为某种补钙剂“钙尔奇”说明书的一部分.取1片钙尔奇,放入盛有10g稀盐酸的烧杯中,其中碳酸钙跟盐酸恰好完全反应(其它成分与盐酸不反应).烧杯内物质质量变为11.34g.(反应方程式:CaCO3+2HCl═CaCl2+H2O+CO2↑)
钙是维持人体正常功能所必需的元素.图为某种补钙剂“钙尔奇”说明书的一部分.取1片钙尔奇,放入盛有10g稀盐酸的烧杯中,其中碳酸钙跟盐酸恰好完全反应(其它成分与盐酸不反应).烧杯内物质质量变为11.34g.(反应方程式:CaCO3+2HCl═CaCl2+H2O+CO2↑)