题目内容
已知氢氧化钠溶液与碳酸氢钙溶液反应的化学方程式为:2NaOH+Ca(HCO3)2=Na2CO3+CaCO3↓+2H2O试计算:
(1)生成的碳酸钙的质量;
(2)反应后所得溶液的溶质质量分数.
设生成碳酸钙的质量为x,生成碳酸钠的质量为y
2NaOH+Ca(HCO3)2=Na2CO3+CaCO3↓+2H2O
80 106 100
4g x y
| 80 |
| 4g |
| 106 |
| y |
| 80 |
| 4g |
| 100 |
| y |
所以反应后所得碳酸钠溶液的溶质质量分数是:
| 5.3g |
| 40.0g +60.0g-5.0g |
答:(1)生成碳酸钙5.0g;
(2)反应后所得碳酸钠溶液的溶质质量分数约是5.6%.

下表列出了两种固体物质的溶解度,回答下列问题:
|


|
0oC |
10 oC |
20 oC |
30 oC |
40 oC |
||||||||||||||
|
A |
37.4g |
36.0g |
34.7 g |
33.8 g |
33.2 g |
||||||||||||||
|
B |
13.3 g |
20.9 g |
31.6 g |
45.8 g |
63.9 g |
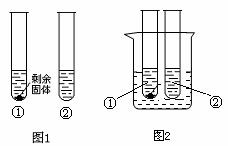
(1)10℃时,取A、B两种固体各3.5g,分别放入10g水中充分溶解,有如图1所示的实验现象,

试管①中溶解的物质是 (填“A”或“B”),其溶液中溶质的质量分数为 (精确到0.1%)。将两只试管同时放入盛有水的烧杯中(如图2),
向烧杯中加入足量NaOH固体并轻轻搅拌,观察到两个试管中的现象分别是:
试管① ;
试管② 。
(2)若向烧杯中加入适量下列物质,两试管中的现象与加NaOH固体相同是 。
A.冰 B.氯化钠 C.生石灰 D.硝酸铵
下表列出了两种固体物质的溶解度,回答下列问题:
|
| 0oC | 10 oC | 20 oC | 30 oC | 40 oC | ||||||||||||||
| A | 37.4g | 36.0g | 34.7 g | 33.8 g | 33.2 g | ||||||||||||||
| B | 13.3 g | 20.9 g | 31.6 g | 45.8 g | 63.9 g |
(1)B为硝酸钾,硝酸钾溶液中的溶剂是 。
(2)将硝酸钾的不饱和溶液变为饱和溶液的方法有 。
(3)10 oC时,取A、B两种固体各35g,分别放入100g水中充分溶解,有如图所示的实验现象,
试管①中溶解的物质是 (填“A”或“B”),其溶液中溶质的质量分数为 (保留一位小数),将两只试管分别放入盛有水的烧杯中(图2),向烧杯中加入足量NaOH并轻轻搅拌,观察到
。
(4)若向烧杯中加入适量下列物质,两试管中的现象与加NaOH不同的是
 A.冰 B.干冰 C.生石灰 D.硝酸铵
A.冰 B.干冰 C.生石灰 D.硝酸铵
下表列出了两种固体物质的溶解度,回答下列问题:
|

| 0oC | 10 | 20 oC | 30 oC | 40 oC | ||||||||||||||
| A | 37.4g | 36.0g | 34.7 g | 33.8 g | 33.2 g | ||||||||||||||
| B | 13.3 g | 20.9 g | 31.6 g | 45.8 g | 63.9 g |
(1)10℃时,取A、B两种固体各3.5g,分别放入10g水
中充分溶解,有如图1所示的实验现象,试管①中溶解的
物质是 (填“A”或“B”),其溶液中溶质的质
量分数为 (精确到0.1%)。将两只试管同时放入盛有水的烧杯中(如图2),
向烧杯中加入足量NaOH固体并轻轻搅拌,观察到两个试管中的现象分别是:
试管① ![]()
![]() ;
;
试管② 。
(2)若向烧杯中加入适量下列物质,两试管中的现象与加NaOH固体相同是 。
A.冰 B.氯化钠 C.生石灰 ![]()
![]() D.硝酸铵
D.硝酸铵
