题目内容
测得某溶液中Cu2-,K+,SO42-,Cl四种离子,且阳离子的个数比为Cu2-:K+=3:4,则
与Cl-的个数比可能是( )
| SO | 2- 4 |
分析:根据溶液中阳离子所带的正电荷总数等于阴离子所带的负电荷总数,据此进行分析解答.
解答:解:溶液中Cu2+与K+的个数比为3:4,设Cu2+和K+个数分别为3n和4n,则溶液中正电荷总数为3n×2+4n×1=10n个;根据溶液中阳离子所带的正电荷总数等于阴离子所带的负电荷总数,负电荷总数也必须为10n个;设
与Cl-的个数比x:y,则2x+y=10n,然后将答案分别代入可知x:y=1:8时负电荷总数能达到10n个.
故选C.
| SO | 2- 4 |
故选C.
点评:本题难度不大,掌握在溶液中阳离子所带的正电荷总数等于阴离子所带的负电荷总数是正确解答此类题的关键.

练习册系列答案
相关题目
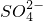 ,Cl四种离子,且阳离子的个数比为Cu2-:K+=3:4,则
,Cl四种离子,且阳离子的个数比为Cu2-:K+=3:4,则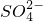 与Cl-的个数比可能是
与Cl-的个数比可能是 ,Cl四种离子,且阳离子的个数比为Cu2-:K+=3:4,则
,Cl四种离子,且阳离子的个数比为Cu2-:K+=3:4,则 与Cl-的个数比可能是( )
与Cl-的个数比可能是( )