题目内容
15. 如图是课堂中模拟炼铁的实验装置.工业上常用一氧化碳还原赤铁矿石来炼铁,试写出炼铁主要反应方程式:3CO+Fe2O3 $\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
如图是课堂中模拟炼铁的实验装置.工业上常用一氧化碳还原赤铁矿石来炼铁,试写出炼铁主要反应方程式:3CO+Fe2O3 $\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;(1)硬质玻璃管中的现象为红色物质逐渐变成黑色,装有澄清石灰水的试管中的现象为澄清石灰水变浑浊,试管中发生反应的方程式为Ca(OH)2+CO2=CaCO3↓+H2O;
(2)实验开始时,先要进行的是Ⅱ(填Ⅰ或Ⅱ)
(3)Ⅰ.加热Ⅱ.通一氧化碳
(4)实验过程中,发现玻璃管炸裂,经检查分析造成此次实验失败的原因是一操作顺序错误所致,请你帮他说明先停止通一氧化碳,后撤酒精喷灯.
(5)该实验设计的不足之处是没有尾气处理.
分析 根据炼铁原理及实验装置图可得出:该实验用一氧化碳还原氧化铁,先排尽装置中的空气,用澄清石灰水来检验产物二氧化碳.通入一氧化碳过量,存在有毒尾气未处理的缺陷.实验中的安全问题是本题的重点考查内容.同时考查了实验现象和反应化学方程式的书写.
解答 解:一氧化碳和氧化铁在高温的条件下反应生成铁和二氧化碳,化学方程式为:3CO+Fe2O3 $\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(1)硬质玻璃管中的现象为:红色物质逐渐变成黑色,二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,所以装有澄清石灰水的试管中的现象为:澄清石灰水变浑浊,化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O;
(2)为防止CO与空气混合加热时引起爆炸,进行加热前要先通入CO排出装置内空气.故实验过程中,先要进行的是Ⅱ;
(3)实验过程中,发现玻璃管炸裂,经检查分析造成此次实验失败的原因是:先停止通一氧化碳,后撤酒精喷灯;
(4)尾气中含有毒气体CO没经处理直接排放到空气中,这是此实验中的不足,应加以改进.
故答案为:3CO+Fe2O3 $\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(1)红色物质逐渐变成黑色,澄清石灰水变浑浊,Ca(OH)2+CO2=CaCO3↓+H2O;
(2)Ⅱ;
(3)先停止通一氧化碳,后撤酒精喷灯;
(4)没有尾气处理.
点评 本题主要对一氧化碳还原氧化铁的实验的相关知识进行了考查,该实验是中考的热点,要加强训练.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.为减少污染、提高利用率,可将煤转化为可燃性气体,其微观示意图如图所示,下列说法正确的是( )

| A. | 图中表示化合物的是“ ” ” | |
| B. | 该反应类型为化合反应 | |
| C. | 反应前后原子的种类和数目保持不变 | |
| D. | 该反应中反应物两种分子的个数比为3:1 |
20.观察与实验是学习化学的重要手段和方法,下列实验对应的描述不合理的是( )
| 实验内容 | 操作或现象 | 解释或结论 | |
| A | 铁丝在充满氧气的集气瓶中燃烧 | 火星四射,并有黑色固体生成 | 黑色固体是氧化铁 |
| B | 将氧化铜与碳粉混合高温加热 | 有红色物质生成 | 说明碳具有还原性 |
| C | 用烧杯取井水20mL,加入少量肥皂水 | 搅拌,产生的泡沫较少,水面 有浮渣 | 该井水是硬水 |
| D | 6000L氧气在加压的情况下 | 可装入容积为40L的钢瓶中 | 分子之间有间隔 |
| A. | A | B. | B | C. | C | D. | D |
7.下列实验操作错误的是( )
| A. |  取用固体粉末 | B. |  读取液体体积 | C. |  熄灭酒精灯 | D. |  洗涤试管 |
5.长久使用的热水壶底部有一层水垢,主要成分是碳酸钙(CaCO3),某化学兴趣小组为了测定水垢中碳酸钙的质量分数,取25g水垢放入过量的稀盐酸的烧杯中,立即将烧杯放在天平上,称其质量.在以后的5min内,每一分钟读一次数.结果如下表,试回答下列问题:
(1)反应生成的二氧化碳的质量为多少?
(2)该水垢中CaCO3的质量分数为多少?
| 时间/min | 1 | 2 | 3 | 4 | 5 |
| 质量/g | 100g | 95g | 92g | 91.2g | 91.2g |
(2)该水垢中CaCO3的质量分数为多少?
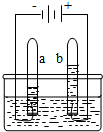 如图电解水的实验中,a试管产生的气体是氢气;b试管产生的气体是氧气;若a试管得到lOmL气体,则b试管可收集到5mL气体,变化前后,物质改变,因而属于化学变化.根据上述实验可以得出:水是由氢元素和氧元素组成的.该反应的文字表达式为:水$\stackrel{通电}{→}$氢气+氧气.在电解水之前往往向水中加入适量的氢氧化钠或稀硫酸的目的是增强水的导电性.
如图电解水的实验中,a试管产生的气体是氢气;b试管产生的气体是氧气;若a试管得到lOmL气体,则b试管可收集到5mL气体,变化前后,物质改变,因而属于化学变化.根据上述实验可以得出:水是由氢元素和氧元素组成的.该反应的文字表达式为:水$\stackrel{通电}{→}$氢气+氧气.在电解水之前往往向水中加入适量的氢氧化钠或稀硫酸的目的是增强水的导电性.
