题目内容
25、现有一包白色粉末,可能由NaCl、Na2SO4、Na2CO3、CuSO4中的一种或几种组成.现做如下实验:①取少量粉末,加水溶解得无色溶液;②另取少量粉末,滴加稀盐酸,无明显现象.请回答:
(1)由上述实验可确定原粉末中一定没有
(2)为进一步确定原粉末的组成,另取少量粉末按下图所示进行实验:
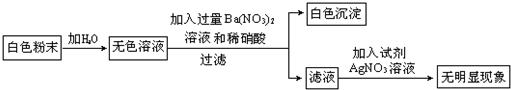
请用化学式表示原粉末的成分
(1)由上述实验可确定原粉末中一定没有
CuSO4、Na2CO3
;可能含有的物质是NaCl、Na2SO4
.(2)为进一步确定原粉末的组成,另取少量粉末按下图所示进行实验:

请用化学式表示原粉末的成分
Na2SO4
;写出有关化学方程式Na2SO4+Ba(NO3)2═BaSO4↓+2NaNO3
;上述实验中,无色溶液中加入的Ba(NO3)2溶液不能用BaCl2溶液取代,原因是用BaCl2溶液会干扰对NaCl的检验
.分析:(1)硫酸铜溶于水产生蓝色溶液,根据①取少量粉末,加水溶解得无色溶液,可以判断白色粉末中没有硫酸铜;而碳酸钠能够跟盐酸反应生成二氧化碳气体,而;②另(2)硫酸钠可以和硝酸钡产生不溶于酸的硫酸钡沉淀,所以根据实验中加入硝酸钡和稀硝酸后产生了白色沉淀,可以判断一定含有硫酸钠,而氯化钠可以和硝酸银反应生成白色的沉淀,根据向滤液中加入硝酸银没有现象,可以断定不含氯化钠,取少量粉末,滴加稀盐酸,无明显现象,可以判断该白色粉末中不含有碳酸钠;
解答:解:(1)硫酸铜溶于水产生蓝色溶液,碳酸钠可以和盐酸反应生成气体,而实验中得到的是无色溶液,且加入盐酸后也没有明显的现象,所以可以得出该白色粉末中一定没有硫酸铜和碳酸钠,故白色粉末可能含硫酸钠和氯化钠的一种或两种;
(2)硫酸钠可以和硝酸钡产生不溶于酸的硫酸钡沉淀,所以根据实验中加入硝酸钡和稀硝酸后产生了白色沉淀,可以判断一定含有硫酸钠,而氯化钠可以和硝酸银反应生成白色的沉淀,根据向滤液中加入硝酸银没有现象,可以断定不含氯化钠,注意在鉴定硫酸钠和氯化钠时,为了防止氯离子干扰实验,应该加入硝酸钡来检验硫酸钠.
故答案为:(1)CuSO4、Na2CO3;NaCl、Na2SO4;
(2)Na2SO4;Na2SO4+Ba(NO3)2═BaSO4↓+2NaNO3 ;用BaCl2溶液会干扰对NaCl的检验.
(2)硫酸钠可以和硝酸钡产生不溶于酸的硫酸钡沉淀,所以根据实验中加入硝酸钡和稀硝酸后产生了白色沉淀,可以判断一定含有硫酸钠,而氯化钠可以和硝酸银反应生成白色的沉淀,根据向滤液中加入硝酸银没有现象,可以断定不含氯化钠,注意在鉴定硫酸钠和氯化钠时,为了防止氯离子干扰实验,应该加入硝酸钡来检验硫酸钠.
故答案为:(1)CuSO4、Na2CO3;NaCl、Na2SO4;
(2)Na2SO4;Na2SO4+Ba(NO3)2═BaSO4↓+2NaNO3 ;用BaCl2溶液会干扰对NaCl的检验.
点评:熟练掌握常见离子溶液的颜色;需要注意混合物中Cl-和SO42-的检验顺序:由于Ag+和SO42-能形成微溶于水的硫酸银造成溶液浑浊,干扰了溶液中Cl-的检验,一定要先检验SO42-再检验Cl-.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目