题目内容
16.N(NO2)3是科学家2011年发现的一种新型火箭燃料.(1)N(NO2)3的相对分子质量是152;
(2)N(NO2)3中氮原子和氧原子的个数比为2:3(填最简比);
(3)1吨N(NO2)3燃料中含氮元素的质量为0.37吨.(准确到小数点后两位)
(4)下列化合物中,氮元素质量分数最小的是C(填字母)
A、N(NO2)3 B、N2O3 C、N2O5.
分析 (1)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.
(2)根据1个N(NO2)3分子的构成进行分析解答.
(3)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
(4)根据化合物中元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%,可将各化学式进行变形,将氮原子个数均变为1个,变形后每个分子中均只含一个氮原子,与氮原子结合的另一种原子的相对原子质量之和越大,氮元素的质量分数越小,进行分析解答.
解答 解:(1)N(NO2)3的相相对分子质量=14×4+16×6=152.
(2)1个N(NO2)3分子中含有4个氮原子和6个氧原子,则N(NO2)3中氮原子和氧原子的个数比为4:6=2:3.
(3)1吨N(NO2)3燃料中含氮元素的质量为1t×$\frac{14×4}{152}×$100%≈0.37t.
(4)将化学式进行变形,将氮原子个数均变为1个,则变形后的化学式分别是NO1.5、N01.5、NO2.5;变形后各选项中每个分子中均只含一个氮原子,与氮原子结合的另一种原子的相对原子质量之和越大,氮元素的质量分数越小;NO2.5中氧元素的质量分素之和最大,则氮元素的质量分数最小.
故答案为:(1)152;(2)2:3;(3)0.37;(4)C.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案
相关题目
13.某学生俯视量取30mL的水,倒掉部分以后,仰视读数是8mL,倒掉的水是( )
| A. | 大于22 mL | B. | 等于22 mL | C. | 小于22 mL | D. | 等于23 mL |
7.化合物Na2PbO3中Pb的化合价为多少( )
| A. | +4 | B. | +6 | C. | -4 | D. | +2 |
11.如图表示自来水消毒过程中发生反应的微观过程,下列叙述正确的是( )
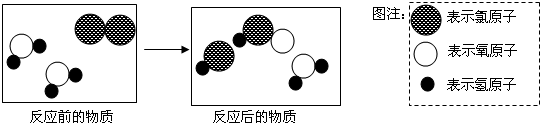

| A. | 化学反应的实质是分子破裂和原子的重新组合 | |
| B. | 生成物中有三种不同的分子 | |
| C. | 反应物中无单质 | |
| D. | 反应前后元素化合价均无变化 |
1.现有Zn、Fe2O3、MgCl2、Cu(OH)2、稀H2SO4等五种物质,在常温下它们两两相互发生的化学反应有( )
| A. | 3个 | B. | 4个 | C. | 5个 | D. | 6个 |
8.下列物质的用途不合理的是( )
| A. | 氢氧化钠用于治疗胃酸过多 | B. | 纯碱溶液用于洗去钢板表面的油污 | ||
| C. | 食醋用于除去热水瓶胆内的水垢 | D. | 生铁用于制造炒菜的锅 |
 回答下列问题:
回答下列问题: