题目内容
11.某无色溶液可使紫色石蕊试纸变红,该溶液中还能大量共存的离子组为( )| A. | NH4+、Na+、Cl-、CO32- | B. | B、Na+、K+、Cu2+、Cl- | ||
| C. | K+、Cl-、Mg2+、SO42- | D. | Ag+、NO3-、Mg2+、Cl- |
分析 某无色溶液可使紫色石蕊试纸变红,说明该溶液显酸,水溶液中含有大量的H+.根据复分解反应的条件,离子间若能互相结合成沉淀、气体或水,则离子不能大量共存,还要注意是无色溶液,不能含有明显有颜色的铜离子、铁离子和亚铁离子等.
解答 解:某无色溶液可使紫色石蕊试纸变红,说明该溶液显酸,水溶液中含有大量的H+.
A、H+在溶液中与CO32-结合生成水和二氧化碳,不能大量共存,故选项错误.
B、四种离子在溶液中不能结合生成沉淀、气体、水,能在酸性溶液中大量共存,但Cu2+的水溶液显蓝色,故选项错误.
C、四种离子在溶液中不能结合生成沉淀、气体、水,能在酸性溶液中大量共存,故选项正确.
D、Ag+、Cl-溶液中与H+结合生成氯化银白色沉淀,不能大量共存,故选项错误.
故选:C.
点评 本题考查了离子共存的问题,判断各离子在溶液中能否共存,主要看溶液中的各离子之间能否发生反应生成沉淀、气体、水;还要注意是在酸性溶液中共存;还要注意特定离子的颜色.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案
相关题目
3.下列变化过程中只发生了物理变化的是( )
| A. | 动植物呼吸 | B. | 食醋除水垢 | C. | 干冰升华 | D. | SO2形成酸雨 |
19.鉴别下列各组物质,所选用的试剂正确的是C
| 被鉴别的物质 | 选用试剂 | |
| A | 氢氧化钠溶液和澄清石灰水 | 稀盐酸 |
| B | 氯化钠溶液和稀盐酸 | 无色酚酞 |
| C | 硝酸铵固体和氢氧化钠固体 | 水 |
| D | 氯化钾固体与硫酸铵固体 | 氢氧化钙 |
6.某同学对一瓶长期暴漏在空气中的氢氧化钠固体样品的成分及含量进行探究.
【提出问题】该样品中含有哪些物质?
【提出猜想】通过分析,提出如下猜想:
猜想Ⅰ:已完全变质,该样品中只含Na2CO3;
猜想Ⅱ:部分变质,该样品中含有NaOH和Na2CO3.
则NaOH变质反应的化学方程式为CO2+2NaOH=Na2CO3+H2O;
【查阅资料】
①碱性的Na2CO3溶液可以与中性的CaCl2溶液发生复分解反应;
②CO2在饱和碳酸氢钠溶液汇总几乎不溶解.
【实验探究】为确定该样品的成分,小明设计了如下实验方案,请你一起完成下列实验报告.
【提出问题2】怎样提纯该样品得到纯净的氢氧化钠固体?
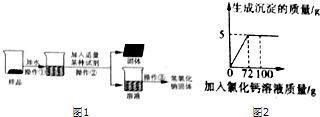
【实验探究2】为得到纯净的氢氧化钠固体,小亮明设计了如图1所示的实验流程.请回答下列问题:
(1)该实验中发生反应的化学方程式为Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;
(2)最终所得氢氧化钠固体质量大于(填“大于”、“等于”或“小于”)变质后样品中氢氧化钠的质量.
【实验反思】
(1)通过本题,你学会了定性检验氢氧化钠的变质和除杂提纯物质.为了得到可靠的实验结果,探究过程中你需要思考的问题有①②④⑤⑥(填数字序号);
①选择试剂种类 ②确定试剂用量 ③试剂产地 ④实验装置与步骤的设计 ⑤实验安全环保 ⑥测量中减少误差.
(2)向50g Na2co3溶液总逐滴加入一定溶质质量分数的CaCl2溶液,实验过程中,生成沉淀的质量与加入CaCl2溶液的质量关系如图所示,试计算:恰好完全反应时,所得溶液中溶质的质量分数.
【提出问题】该样品中含有哪些物质?
【提出猜想】通过分析,提出如下猜想:
猜想Ⅰ:已完全变质,该样品中只含Na2CO3;
猜想Ⅱ:部分变质,该样品中含有NaOH和Na2CO3.
则NaOH变质反应的化学方程式为CO2+2NaOH=Na2CO3+H2O;
【查阅资料】
①碱性的Na2CO3溶液可以与中性的CaCl2溶液发生复分解反应;
②CO2在饱和碳酸氢钠溶液汇总几乎不溶解.
【实验探究】为确定该样品的成分,小明设计了如下实验方案,请你一起完成下列实验报告.
| 实验操作 | 实验现象 | 实验结论 |
| (1)取少量样品溶于水,加入 过量CaCl2溶液; | 白色沉淀产生 | 该反应的化学方程式:Na2CO3+CaCl2═2NaCl+CaCO3↓ |
| (2)将上述反应后的混合液过滤,取滤液加入酚酞试液; | 溶液变红色 | 证明猜想Ⅱ正确 |
【实验探究2】为得到纯净的氢氧化钠固体,小亮明设计了如图1所示的实验流程.请回答下列问题:
(1)该实验中发生反应的化学方程式为Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;
(2)最终所得氢氧化钠固体质量大于(填“大于”、“等于”或“小于”)变质后样品中氢氧化钠的质量.
【实验反思】
(1)通过本题,你学会了定性检验氢氧化钠的变质和除杂提纯物质.为了得到可靠的实验结果,探究过程中你需要思考的问题有①②④⑤⑥(填数字序号);
①选择试剂种类 ②确定试剂用量 ③试剂产地 ④实验装置与步骤的设计 ⑤实验安全环保 ⑥测量中减少误差.
(2)向50g Na2co3溶液总逐滴加入一定溶质质量分数的CaCl2溶液,实验过程中,生成沉淀的质量与加入CaCl2溶液的质量关系如图所示,试计算:恰好完全反应时,所得溶液中溶质的质量分数.

20.关于过氧化氢(H2O2)的叙述中,正确的是( )
| A. | 由氢氧两种元素组成的化合物 | |
| B. | 由一个个水分子和一个氧原子构成 | |
| C. | 过氧化氢分子由氢分子和氧分子构成 | |
| D. | 其中氢元素和氧元素之间的质量比为1:1 |
 哈尔滨漫长而寒冷的冬季,人们常常使用填充棉花的棉衣来保暖.
哈尔滨漫长而寒冷的冬季,人们常常使用填充棉花的棉衣来保暖.