题目内容
13、Al与NaOH溶液反应的化学方程式为2Al+2NaOH+2H2O=2NaAlO2+3X↑
(1)根据质量守恒定律,试推断X的化学式为
(2)NaAlO2中Al的化合价为
(1)根据质量守恒定律,试推断X的化学式为
H2
.(2)NaAlO2中Al的化合价为
+3
.分析:(1)根据化学变化前后原子的种类、数目不变,由反应的化学方程式2Al+2NaOH+2H2O=2NaAlO2+3X↑,可以推断反应中物质X的分子构成及物质X化学式的确定;
(2)根据化合物中各元素化合价代数和为0,由物质的化学式NaAlO2,计算其中Al元素的化合价.
(2)根据化合物中各元素化合价代数和为0,由物质的化学式NaAlO2,计算其中Al元素的化合价.
解答:解:(1)由反应的化学方程式2Al+2NaOH+2H2O=2NaAlO2+3X↑,
反应前 反应后
Al原子 2 2
Na原子 2 2
O原子 4 4
H原子 6 0
根据化学变化前后原子的种类、数目不变,可判断物质X的每个分子由2个H原子构成,则物质X的化学式为H2;
故答案为:H2;
(2)设化合物NaAlO2中Al元素的化合价为x,依据化合物中各元素的化合价为0,则(+1)+x+(-2)×2=0,解得x=+3;
故答案为:+3.
反应前 反应后
Al原子 2 2
Na原子 2 2
O原子 4 4
H原子 6 0
根据化学变化前后原子的种类、数目不变,可判断物质X的每个分子由2个H原子构成,则物质X的化学式为H2;
故答案为:H2;
(2)设化合物NaAlO2中Al元素的化合价为x,依据化合物中各元素的化合价为0,则(+1)+x+(-2)×2=0,解得x=+3;
故答案为:+3.
点评:根据化学变化前后原子的种类、数目不变,由反应的化学方程式,可以推断反应中某物质的分子构成及物质化学式的确定.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
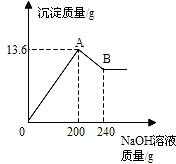 把MgCl2、AlCl3两种固体组成的混合物溶于足量的水后,在所得溶液中逐滴加入10%的NaOH溶液,加入NaOH溶液的质量和生成沉淀的质量如下图所示.已知:NaOH与AlCl3反应时,先使AlCl3全部转化为不溶于水的Al(OH)3,然后Al(OH)3还能继续与过量的NaOH发生如下反应:Al(OH)3+NaOH═NaAlO2+2H2O,其中NaAlO2 是可溶于水的物质,试回答:
把MgCl2、AlCl3两种固体组成的混合物溶于足量的水后,在所得溶液中逐滴加入10%的NaOH溶液,加入NaOH溶液的质量和生成沉淀的质量如下图所示.已知:NaOH与AlCl3反应时,先使AlCl3全部转化为不溶于水的Al(OH)3,然后Al(OH)3还能继续与过量的NaOH发生如下反应:Al(OH)3+NaOH═NaAlO2+2H2O,其中NaAlO2 是可溶于水的物质,试回答: