题目内容
取氯酸钾和二氧化锰的混合物12克制取氧气,加热一段时间后,测得50%的氯酸钾分解,将剩余的固体冷却后称量,其质量为10.08克,求原混合物中氯酸钾和二氧化锰各多少克?
【答案】
9.8g;?? 2.2g
【解析】
试题分析:由于两次称重都是固体的质量,且有差值.而根据质量守恒定律,前后质量一定相等,所以必然过程中生成气体或者液体,由于是氯酸钾和二氧化锰的混合物,所以会生成氧气,所以气体氧气的质量就等于:12g-10.08g=1.92g.
设生成1.92g氧气时参与反应的氯酸钾的质量为x,
2KClO3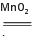 2KCl + 3O2 ↑
2KCl + 3O2 ↑
245 ????????? 96
X ??????? 1.92g,
245:96=X:1.92g
解之得:x=4.9g
由于是氯酸钾只是分解了50%,所以原混合物中氯酸钾的质量为:4.9g÷50%=9.8g;
由于反应前的混合物的总质量为12g,所以原混合物中二氧化锰的质量为:12g-9.8g=2.2g.
答:原混合物中氯酸钾有9.8克;二氧化锰有2.2克.
考点:根据化学方程式的计算

练习册系列答案
相关题目