题目内容
现有100mL质量分数为20%的硫酸溶液,其密度为1.14g/cm3,下列说法正确的是
[ ]
A.该溶液含溶质20g
B.该溶液中,溶质质量∶溶液质量=1∶6
C.该溶液中,溶质质量∶溶剂质量=1∶5
D.该溶液中,溶液质量∶溶剂质量=5∶4
答案:D
解析:
提示:
解析:
|
精析 该溶液中溶质质量为100mL×1.14g/mL×20%=22.8g.溶质质量分数为20%可以理解为 |
提示:
|
总结:此题要求深刻理解溶质质量分数的含义和公式,并会灵活地对公式作如下变形:溶质质量=溶液质量×溶质质量分数=溶液密度×体积×溶质质量分数. |

练习册系列答案
相关题目
(8分)(2012?南通)维生素C是一种人体必需的维生素.查阅资料可知下列信息:
| | 部分性质 | 生理作用 |
| 维生素C 化学式:C6H806 | 无色晶体,易溶于水;在酸性溶液 中稳定,中性或碱性溶液中易被空气氧化… | 促进人体生长发育,增强人体对 疾病的抵抗能力… |
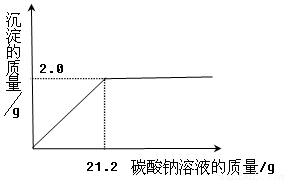
(2)某兴趣小组的同学对维生素C的还原性进行实验探究,其实验结果如下图所示.实验说明了维生素C在空气中氧化除跟氧气有关外,还与 _________ 有关.因此,生吃新鲜蔬菜要比熟吃蔬菜维生素C的损失 _________ (选填“大”或“小”).
(3)①该兴趣小组同学对某果计饮料中维生素C的含量进行测定,反应原理为:C6H806+I2═C6H606+2HI
实验步骤如下:
a.取果汁饮料10mL,用煮沸并冷却的蒸馏水稀释到50mL
b.加醋酸溶液酸化
c.加入少量指示剂
d.逐滴加入稀碘水至完全反应,实验测得恰好反应时,消耗溶质碘的质量为25.4mg.计算该果汁饮料每100mL中含维生素C的质量为多少mg?(请将计算过程写在答题卡上)
②有些同学在测定时,未加入醋酸溶液酸化,测得维生素C的含量明显小于其他同学.
其原因是 _________ .

 17、现有实验药品:一定质量的锌 (片状或粒状)、浓硫酸和水.如右图所示装置.图中量气管是由B、C两根玻璃管组成,它们用橡皮管连通,并装适量水,B管有刻度(0-100mL),B、C管可固定在铁架台上,供量气用;C管可上下移动,以调节液面高低.利用此装置将锌与稀硫酸反应可测定锌的相对原子质量(设锌全部反应,产生的气体不超过50mL).
17、现有实验药品:一定质量的锌 (片状或粒状)、浓硫酸和水.如右图所示装置.图中量气管是由B、C两根玻璃管组成,它们用橡皮管连通,并装适量水,B管有刻度(0-100mL),B、C管可固定在铁架台上,供量气用;C管可上下移动,以调节液面高低.利用此装置将锌与稀硫酸反应可测定锌的相对原子质量(设锌全部反应,产生的气体不超过50mL).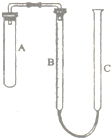 现有实验药品:一定质量的锌(片状或粒状)、浓硫酸(密度1.84g/cm3)、水以及如图所示装置.图中量气管是由B、C两根玻璃管组成,它们用橡皮管连通,并装适量水,B管有刻度(0-100mL),B、C管可固定在铁架上,供量气用;C管可上下移动,以调节液面高低.利用此装置可测定锌的相对原子质量.(设锌全部反应,产生的气体不超过50mL).
现有实验药品:一定质量的锌(片状或粒状)、浓硫酸(密度1.84g/cm3)、水以及如图所示装置.图中量气管是由B、C两根玻璃管组成,它们用橡皮管连通,并装适量水,B管有刻度(0-100mL),B、C管可固定在铁架上,供量气用;C管可上下移动,以调节液面高低.利用此装置可测定锌的相对原子质量.(设锌全部反应,产生的气体不超过50mL).