题目内容
18.图1为氯化钠、碳酸钠在水中的溶解度曲线.请回答下列问题:
(1)30℃时,氯化钠的溶解度=碳酸钠的溶解度(填写“>”、“<”或“=”);
(2)10℃时,向两只盛有100g水的烧杯中,分别加入氯化钠、碳酸钠两种物质,至不再溶解为止,其中
氯化钠(填溶质)质量较大.
(3)生活在盐湖附近的人们习惯“夏天晒盐,冬天捞碱”.
请你解释原因:碳酸钠的溶解度受温度影响变化较大,氯化钠的溶解度受温度影响变化较小.
(4)如图2所示,20℃时,将盛有饱和碳酸钠溶液的小试管放入盛水的烧杯中,向水中加入某物质后,试管中有晶体析出.加入的物质可能是C(填字母序号).
A.氢氧化钠 B.氯化钠 C.硝酸铵 D.浓硫酸.
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)通过分析溶解度曲线可知,30℃时,氯化钠的溶解度=碳酸钠的溶解度;
(2)10℃时,氯化钠的溶解度大于碳酸钠的溶解度,所以向两只盛有100g水的烧杯中,分别加入氯化钠、碳酸钠两种物质,至不再溶解为止,其中氯化钠质量较大;
(3)生活在盐湖附近的人们习惯“夏天晒盐,冬天捞碱”,原因是:碳酸钠的溶解度受温度影响变化较大,氯化钠的溶解度受温度影响变化较小;
(4)由饱和碳酸钠溶液的小试管放入盛水的烧杯中,向水中加入某物质后,试管中有晶体析出,说明温度降低了,也就是说该物质溶于水是吸热的,所以为硝酸铵,故选:C.
故答案为:(1)=;
(2)氯化钠;
(3)碳酸钠的溶解度受温度影响变化较大,氯化钠的溶解度受温度影响变化较小;
(4)C.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
相关题目
3.分类是学习和研究化学的常用方法.下列分类中正确的是( )
| A. | 合成材料:塑料、合成橡胶、合成纤维 | |
| B. | 碱:火碱、纯碱、消石灰 | |
| C. | 微量元素:钙、铁、锌、硒 | |
| D. | 复合肥:尿素、硝酸钾、磷酸钾 |
7.工业制镁的方法为:将含碳酸钙的贝壳制成石灰乳;在海水中加入石灰乳,过滤;在氢氧化镁中加入盐酸,结晶;电解熔融氯化镁.该方法中的化学反应不包括( )
| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |
8.下列各组物质,从左到右的排列顺序中,没有任何规律的是( )
| A. | KClO3 KClO Cl2 NaCl | B. | HNO3 H2SO4 H3PO4 H4SiO4 | ||
| C. | Mg Zn Fe Cu | D. | NH3 CH4 HCl CaO |
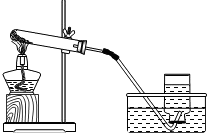 某同学在实验室用以下装置制备氧气并验证氧气的性质.
某同学在实验室用以下装置制备氧气并验证氧气的性质. ;
;