题目内容
【题目】某校化学研究性学习小组在学习了“空气中氧气含量测定”的基础上,改进了教材中的实验,设计出了如图所示的实验装置。实验步骤如下:
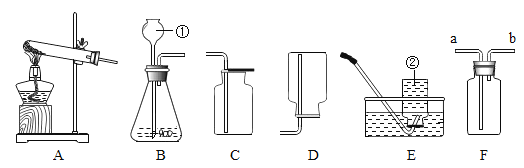
①如图所示,连接仪器,检查装置的气密性。发现装置的气密性良好;
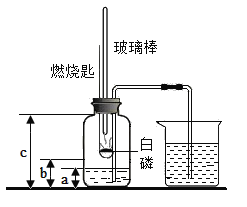
②在集气瓶里装进适量a体积的水,燃烧匙里放一块白磷(白磷燃烧所需要的最低温度是40℃),并在酒精灯上把玻璃棒下端加热,按图示装置把集气瓶中的空气密封起来,把长导管的另一端放入盛有足量水的烧杯中;(注:集气瓶内的长导管已伸到了瓶底)
③用力把预先加热过的玻璃棒按下与白磷接触,_____;(注:白磷与红磷燃烧的产物相同)
④待白磷燃烧熄灭后,稍加振荡,白烟消失;
⑤待集气瓶完全冷却至室温,量出集气瓶中水的体积是b,整个集气瓶的体积是c;
⑥根据a、b、c三个数据,计算出空气中氧气的体积分数。
根据以上信息,回答下列问题:
(1)集气瓶中白磷燃烧的文字表达式_____;
(2)请在步骤③中的“_____”上写上相应的实验现象;
(3)若实验非常成功,当c为500mL,a=100mL,则b=_____mL;
(4)在上述实验中,下列操作的实施和实验现象的出现,会导致实验最后产生的实际值小于理论值的是_____
①白磷的量不足,瓶内氧气没有耗尽
②用等质量的蜡烛代替白磷完成本实验
③装置气密性不好
【答案】磷+氧气![]() 五氧化二磷 白磷燃烧,产生白烟,放出热量 180 ①②③
五氧化二磷 白磷燃烧,产生白烟,放出热量 180 ①②③
【解析】
(1)该实验中白磷燃烧生成了五氧化二磷,发生的化学反应的文字表达式是:磷+氧气![]() 五氧化二磷;
五氧化二磷;
(2)用力把预先加热过的玻璃棒按下与白磷接触,白磷燃烧,产生白烟,放出热量;
(3)由于氧气约占空气体积的1/5;若实验非常成功,测a、b、c三个数据应满足的一个等式关系式:b-a=![]() (c-a);当c为500mL,a=100mL,则b=100mL+400mL×
(c-a);当c为500mL,a=100mL,则b=100mL+400mL×![]() =180mL;
=180mL;
(4)①白磷的量不足,瓶内氧气没有耗尽,实际值小于理论值;
②蜡烛燃烧生成水和二氧化碳,用等质量的蜡烛代替白磷完成本实验,实际值小于理论值;
③装置气密性不好,会导致实验最后产生的实际值小于理论值,实际值小于理论值。故选①②③。

 阅读快车系列答案
阅读快车系列答案【题目】甲、乙两同学想了解碳酸钠溶液的酸碱性。他们做了以下研究:
实 验 操 作 | 检测结果 | |
甲同学 | 取pH试纸放在玻璃片上;用玻璃棒蘸取碳酸钠溶液沾在pH试纸上;将试纸显示的颜色与标准比色卡比较。 | pH>7 |
乙同学 | 将pH试纸直接浸入碳酸钠溶液中,把试纸显示的颜色与标准比色卡比较。 | pH>7 |
(1)碳酸钠的化学式为__________,它属于________(填酸、碱、盐、氧化物)
(2)根据两位同学的实验可得出碳酸钠溶液酸碱性的结论:__________________
(3)根据两位同学的实验操作,你认为_________同学操作不规范。为什么?_____________。
(4)如果实验室没有pH试纸,又要一次测定未知溶液的酸碱性,可选用__________试液来进行实验。
【题目】Ⅰ.小芳发现,氯酸钾与氧化铜混合加热,也能较快产生氧气,于是进行探究:
[提出猜想] 除二氧化锰、氧化铜外,氧化铁也可以作氯酸钾分解的催化剂。
[完成实验] 按下表进测定分解温度(分解温度越低,催化效果越好)。
实验编号 | 实验药品 | 分解温度(℃) |
① | 氯酸钾 | 580 |
② | 氯酸钾、二氧化锰(质量比1︰1) | 350 |
③ | 氯酸钾、氧化铜(质量比1︰1) | 370 |
④ | 氯酸钾、氧化铁(质量比1︰1) | 390 |
(1)由实验_______________与实验④对比,证明猜想合理;
(2)实验所用物质中,催化效果最好的是_______,该反应的化学方程式为________ ;
[反思]
(3)若要证明氧化铁是该反应的催化剂,还要验证它在化学反应前后_______和 ______不变。
Ⅱ.下表是二氧化锰用量与一定质量氯酸钾制取氧气反应速率关系的实验数据:
二氧化锰与氯酸钾的质量比 | 1︰40 | 1︰20 | 1︰10 | 1︰5 | 1︰3 | 1︰2 | 2︰3 | 1︰1 | 2︰1 |
生成1L氧气所需的时间(s) | 124 | 79 | 50 | 54 | 75 | 93 | 106 | 153 | 240 |
(4)据如表可知二氧化锰与氯酸钾的质量比为_______________时,反应速率最快;
(5)通过分析可知,在化学反应中催化剂的用量_______________越多越好。(填“是”或“不是”)