题目内容
8.废铁屑的主要成分是铁,同时还有少量铁锈(Fe2O3),动物饲料硫酸亚铁的生产工艺之一如图所示: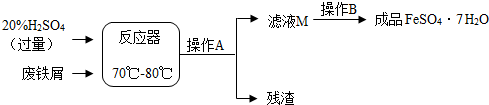
(1)在反应器中发生反应的化学方程式除Fe2(SO4)3+Fe=3FeSO4外还有2个反应,①有单质生成的化学方程式是Fe+H2SO4=FeSO4+H2↑,②没有单质生成的化学方程式是Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;其中同时作为反应器维持70℃~80℃所需热量主要提供者的反应是①(填“①”或“②”);反应器所在的厂房要加强通风的原因可能是稀释具有可燃性的氢气,以防爆炸.
(2)滤液M中肯定含有的溶质的化学式是FeSO4、H2SO4.
(3)滤液M经过操作B可得硫酸亚铁晶体(FeSO4•7H2O).已知硫酸亚铁的溶解度和析出晶体的组成如下表:
| 温度/℃ | 0 | 10 | 30 | 40 | 50 | 60 | 64 | 70 | 80 | 90 |
| 溶解度/g | 15.6 | 20.5 | 33.0 | 40.4 | 48.8 | 55.0 | 55.3 | 50.6 | 43.7 | |
| 析出晶体 | FeSO4•7H2O | FeSO4•4H2O | FeSO4•H2O | |||||||
(4)将无水硫酸亚铁(FeSO4)隔绝空气加强热,生成产物有三氧化二铁和其它两种硫的氧化物,试写出该反应的化学方程式:2FeSO4$\frac{\underline{\;高温\;}}{\;}$Fe2O3+SO2↑+SO3↑.
分析 (1)根据铁、氧化铁都能和稀硫酸反应,可以依据反应物、生成物结合质量守恒定律写出反应的化学方程式;
(2)根据加入的硫酸是过量的,所以在溶液中含有硫酸和反应生成的硫酸亚铁进行分析解答;
(3)根据图表中的信息可以知道当温度大于64℃时产生了FeSO4•4H2O,可以据此解答该题;
(4)根据题给的信息可以判断无水硫酸亚铁(FeSO4)隔绝空气加强热,生成产物有三氧化二铁、二氧化硫和三氧化硫,可以据此写出该反应的化学方程式.
解答 解:(1)通过分析可知,铁和硫酸反应生成了硫酸亚铁和氢气,氧化铁和硫酸反应生成了硫酸铁和水,化学方程式为:Fe+H2SO4═FeSO4+H2↑,Fe2O3+3H2SO4═Fe2(SO4)3+3H2O;活泼金属与酸发生的置换反应过程中会放出热量,因为反应中产生了具有可燃性的氢气,所以要通风,以防发生爆炸;
故填:Fe+H2SO4=FeSO4+H2↑;Fe2O3+3 H2SO4=Fe2(SO4)3+3H2O;①;稀释具有可燃性的氢气,以防爆炸;
(2)加入的硫酸是过量的,所以在溶液中含有硫酸和反应生成的硫酸亚铁,所以滤液M中肯定含有的溶质的化学式是:FeSO4、H2SO4;
故填:FeSO4、H2SO4;
(3)根据图表中的信息可以知道当温度大于64℃时产生了FeSO4•4H2O,所以应该将温度控制在64℃以下;
故填:64℃;
(4)根据题给的信息可以判断无水硫酸亚铁(FeSO4)隔绝空气加强热,生成产物有三氧化二铁和三氧化硫,在氧化还原反应中,若有元素的化合价升高,必有元素的化合价降低,且元素化合价升降总数相等,所以结合元素化合价的变化可以知道,铁元素的化合价由+2变成了+3价,所以反应中有二氧化硫生成,硫元素的化合价由+6降低到+4,所以根据质量守恒定律可以判断在该反应中还生成了三氧化硫,所以该反应的化学方程式为:2FeSO4$\frac{\underline{\;高温\;}}{\;}$Fe2O3+SO2↑+SO3↑.
故填:2FeSO4$\frac{\underline{\;高温\;}}{\;}$Fe2O3+SO2↑+SO3↑.
点评 在解此类题时,应掌握化学方程式的书写、盐的化学性质等知识,并学会分析信息、提取信息,并根据所学知识结合所给信息进行解答.

 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案
| A. | 甲试管中收集到的是一种可燃性气体 | |
| B. | 该实验能证明水由氢元素和氧元素组成 | |
| C. | 向水中加入少量硫酸,能增强水的导电性 | |
| D. | a与电源的正极相连 |
| A. | 氮肥不但能促进农作物枝叶茂盛,叶色浓绿,还能提高产量 | |
| B. | CO2的排放是导致酸雨的主要原因 | |
| C. | 合金、塑料、橡胶等都是重要的有机合成材料 | |
| D. | 防止金属腐蚀是保护金属资源的有效途径 |
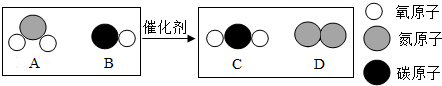
| A. | 反应前后各元素化合价均未改变 | B. | 参加反应的分子个数比为1:1 | ||
| C. | 加入催化剂可提高产物质量 | D. | 利用此反应可减少有毒气体的排放 |