题目内容
13.馒头面包等发面食品的一个特点是面团中有许多小孔,它们使发面食品松软可口.而发酵粉是制作糕点不可缺少的原料.小红对发酵粉产生了兴趣,她查阅资料发现发酵粉的主要成分含碳酸钠、碳酸氢钠,它们可与面粉、水混合发酵产生二氧化碳气体,这些气体会在面团中形成许多小孔使馒头面包松软可口.【猜想】小红认为可用发酵粉与稀盐酸反应制CO2.
【实验探究】小红进行如下探究:
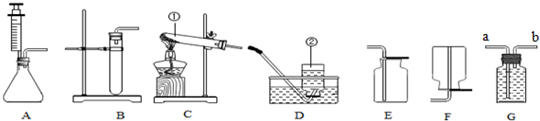
(1)若选择下列仪器组装CO2的发生装置,她应选择的仪器是ADF或CE.(填仪器编号) 说明:F中的橡皮塞为双孔塞.

(2)碳酸钠是发酵粉的主要成分之一.实验时小红忘了稀释浓盐酸,她直接将足量浓盐酸与适量发酵粉反应,观察到反应发生器里反应十分剧烈,有大量气泡冒出.写出发酵粉中碳酸钠与浓盐酸反应的化学方程式Na2CO3+2HCl=2NaCl+H2O+CO2↑.
(3)小红准备用新制的澄清石灰水来验证生成的CO2,她预计观察到的实验现象是澄清石灰水变浑浊.
【反思与评价】在实验(3)中,小红的实验未达到预期结果,请你帮她分析原因.浓盐酸能挥发,挥发出的HCl与Ca(OH)2发生反应.
(4)根据反应现象说明实验室为什么不选用碳酸钠和稀盐酸制备CO2:反应速率过快,不便于收集.
分析 根据反应物状态及反应条件选择发生装置根据书写方程式原则书写方程式根据检验二氧化碳的方法解答根据浓盐酸的挥发性以及反应物的接触面积分析.
解答 解:(1)发酵粉、面粉是固体,水是液体,反应条件是常温,因此选择固液常温型装置,可选用的仪器有ADF 或CE;故填:ADF 或CE;
(2)碳酸钠又名纯碱,与盐酸反应生成氯化钠、水和二氧化碳;化学方程式为Na2CO3+2HCl=2NaCl+H2O+CO2↑;故填:Na2CO3+2HCl=2NaCl+H2O+CO2↑;
(3)二氧化碳与氢氧化钙反应生成碳酸钙沉淀,因此可用澄清石灰水检验二氧化碳,澄清石灰水变浑浊,化学方程式为CO2+Ca(OH)2═CaCO3↓+H2O;故填:澄清石灰水变浑浊;
浓盐酸有挥发性,挥发出的HCl与Ca(OH)2发生反应.因此看不到石灰水变浑浊;故填:浓盐酸能挥发,挥发出的HCl与Ca(OH)2发生反应;
(4)碳酸钠是一种粉末状态药品,与稀盐酸接触面积太大,反应速率过快不便于收集;故填:反应速率过快,不便于收集.
点评 本题考查二氧化碳制取装置,检验方法及药品选择的注意事项,需加强理解与记忆.

练习册系列答案
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案
相关题目
4.下列物质能够导电的是( )
| A. | 固体食盐 | B. | 澄清石灰水 | C. | 糖水 | D. | 蒸馏水 |
8.下列现象能用质量守恒定律解释的是( )
| A. | 水结冰产后质量不变 | |
| B. | 铜粉加热后质量增加了 | |
| C. | 加压降温下氧气变为蓝色液体 | |
| D. | 1升水和1升酒精混合总体积小于2升 |
5.化学上把一种元素组成的不同单质称作同素异形体,下面各组物质是同素异形体的是( )
| A. | 水和过氧化氢 | B. | 氧气和臭氧 | C. | 金刚石和煤炭 | D. | 天然气和甲烷 |
2.下列不能用质量守恒定律解释的是( )
| A. | 鲜牛奶变质 | B. | 粮食酿成酒 | C. | 钢丝球刷碗 | D. | 煤炭的燃烧 |
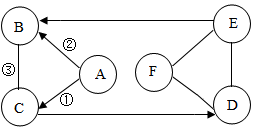 A、B、C、D、E、F都是初中化学常见的物质,A、C都是维系人类生命最重要的物质,B是用于光合作用和灭火的气体,D可用于保护树木,防止冻伤,并防止害虫生卵,E中含有两种元素,它们之间的转化关系如图所示.(“-”表示两端的物质能发生化学反应;“→”表示物质之间的转化关系.)
A、B、C、D、E、F都是初中化学常见的物质,A、C都是维系人类生命最重要的物质,B是用于光合作用和灭火的气体,D可用于保护树木,防止冻伤,并防止害虫生卵,E中含有两种元素,它们之间的转化关系如图所示.(“-”表示两端的物质能发生化学反应;“→”表示物质之间的转化关系.)