题目内容
新型材料纳米级 Fe 粉具有广泛的用途,它比普通 Fe 粉更易与氧气反应,其制备工艺流程如图所示:请回答下列问题:

(1)纳米 级 Fe 粉在氧气中能自发燃烧生成黑色固体,此黑色固体的化学式为 Fe3O4 .
级 Fe 粉在氧气中能自发燃烧生成黑色固体,此黑色固体的化学式为 Fe3O4 .
(2)请补充完成上述制备工艺的化学方程式:H2+FeCl2 Fe+ 2HCl .
Fe+ 2HCl .
在制备纳米级 Fe 粉的工艺流程中,N2的作用是 催化作用 .
(3)研究人员发现最后制得的纳米级 Fe 粉样品中混有少量的 FeCl2 杂质.
①为除去样品中的杂质,在无氧环境下,先加 水 溶解 ,然后再 过滤 、洗涤、烘干.
,然后再 过滤 、洗涤、烘干.
②取样品20g,加入足量的盐酸,生成氢气 0.7g.请计算该样品中单质 Fe 的质量分数.
(请写出计算过程) .
【答案】(1) Fe3O4 .(2) 2HCl 催化作用 (3)① 水 过滤 ②98%.

②设生成0.7g氢气需要参加反应的铁的质量为X,则:
Fe+2HCl═FeCl2+H2↑
56 2
X 0.7g
根据: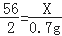 解得X=19.6g.
解得X=19.6g.
铁的质量分数为: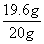 ×100%=98%
×100%=98%
答:略。

 步步高达标卷系列答案
步步高达标卷系列答案金属锌与稀硫酸反应生成硫酸锌和氢气,化学课外小组的同学对“锌与硫酸反应快慢的影响因素”进行了探究。
【提出问题】锌与硫酸反应的快慢受哪些因素的影响呢?
【猜想与假设】a.可能与硫酸的质量分数有关;b.可能与锌的形状有关。
【设计并实验】小组同学用不同质量分数的硫酸和不同形状的锌进行如下实验。
| 实验编号 | 硫酸的质量分数 (均取20mL) | 锌的形状 (均取1g) | 氢气的体积(mL) (均收集3分钟) |
| ① |
| 锌粒 | 31.7 |
| ② | 20% | 锌片 | 50.9 |
| ③ | 30% | 锌粒 | 61.7 |
| ④ | 30% | 锌片 | 79.9 |
 (1)小组同学用右图装置收集并测量氢气的体积,其中量筒的作用是 ,氢气应从 (填e或f或g)管通入。(已知:氢气难溶于水)
(1)小组同学用右图装置收集并测量氢气的体积,其中量筒的作用是 ,氢气应从 (填e或f或g)管通入。(已知:氢气难溶于水)
【收集证据】
(2)要比较不同质量分数的硫酸对反应快慢的影响,应选择的实验编号是 。
【得出结论】
(3)结论是  。
。
【评价与反思】
(4)下表是小 组同学第①组实验的详细数据。
组同学第①组实验的详细数据。
| 时段(均为1分钟) | 第1分钟 | 第2分钟 | 第3分钟 | 第4分钟 | 第5分钟 | 第6分钟 |
| H |
| 16.7mL | 11.9mL | 9.6mL | 7.6mL | 6.0mL |
请描述锌与硫酸反应快慢的变化 ,并解释第二分钟以后变化的原因 。
 (5)锌与硫酸反应的快慢可能还受温度因素的影响,请设计实验验证 。
(5)锌与硫酸反应的快慢可能还受温度因素的影响,请设计实验验证 。

 K2MnO4+MnO2+O2↑)
K2MnO4+MnO2+O2↑)
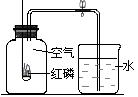 ③夏天,盛放冰棒的杯子外壁上附有一层水珠,说明空气中含有 。
③夏天,盛放冰棒的杯子外壁上附有一层水珠,说明空气中含有 。 (1)指出图中比较明显的错误:
(1)指出图中比较明显的错误: 
 3.1mL
3.1mL