题目内容
200g
稀盐酸与300g碳酸钠溶液恰好完全反应生成二氧化碳8.8g.求:(1)
盐酸溶液中溶质的质量分数;(2)
生成的氯化钠溶液中溶质的质量分数.
答案:7.3%;4.8%

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
长久使用的热水瓶底部有一层水垢,主要成分是碳酸钙,用稀盐酸可以清除水垢.某学校化学课外兴趣小组的同学通过实验测定水垢中碳酸钙的含量,将过量的稀盐酸加到200g水垢中,同时测量4分钟内产生CO2的质量部分结果如下表:[CaCO3+2HCl═CaCl2+H2O+CO2↑]
(1)该小组因故没有记录反应时间为180s时的数
据M.你由表中数据推测,M= g.
(2)反应生成CO2的总质量为 g.(3)根据实验数据,在右边的坐标纸上绘制生成CO2质量与反应时间关系的曲线.你由曲线中推测在反应60s时,生成CO2的质量约为 .
(4)计算水垢中碳酸钙质量分数是多少?
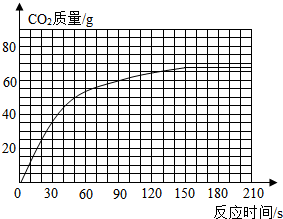
| 时间/s | 30 | 50 | 90 | 150 | 180 | 210 |
| CO2质量/g | 30 | 50 | 60 | 66 | M | 66 |
据M.你由表中数据推测,M=
(2)反应生成CO2的总质量为
(4)计算水垢中碳酸钙质量分数是多少?

长时间使用的热水壶底部有一层水垢,主要成分是CaCO3和Mg(OH)2.学校化学研究性学习小组同学通过实验想测定水垢中CaCO3的含量为多少.他们取200g水垢,加入过量的稀盐酸,同时测量5分钟(min)内生成CO2质量(已知Mg(OH)2与稀盐酸反应不能放出C02气体),测量数据如下表:
计算:(1)3min时,水垢中的CaCO3是否反应完全?请说明理由
(2)该水垢中CaCO3的质量分数是多少?
| 时间/min | 1 | 2 | 3 | 4 | 5 |
| 生成CO2的质量/g | 18 | 25 | 30 | 33 | 33 |
(2)该水垢中CaCO3的质量分数是多少?

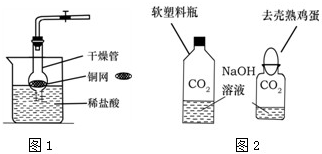 CO2是初中化学重点研究的气体之一.某化学兴趣小组设计了如下实验来探究CO2的制取和性质:
CO2是初中化学重点研究的气体之一.某化学兴趣小组设计了如下实验来探究CO2的制取和性质: