题目内容
在盛有5mL 5%过氧化氢溶液的试管中,加入少量的二氧化锰,反应结束后,下列三项:①过氧化氢的质量 ②水的质量 ③二氧化锰的质量,与反应前相比,其中发生变化的是
- A.仅①
- B.仅②
- C.仅①和②
- D.①②③
C
分析:根据过氧化氢溶液制取氧气的化学反应式可知,过氧化氢被分解成氧气和水,其中二氧化锰的作用是催化剂.然后根据我们了解的这些信息判断①②③的正确与否.
解答:①因过氧化氢被分解成水和氧气,所以过氧化氢的质量一定会发生变化;②水除了原来的,又有水生成,所以水的质量也发生了变化;③二氧化锰是催化剂在反应前后质量和性质都不发生变化.其中发生变化的是①②.
故选C.
点评:了解催化剂的特点是本身在反应前后质量和性质都不发生变化,只是改变反应的速率.
分析:根据过氧化氢溶液制取氧气的化学反应式可知,过氧化氢被分解成氧气和水,其中二氧化锰的作用是催化剂.然后根据我们了解的这些信息判断①②③的正确与否.
解答:①因过氧化氢被分解成水和氧气,所以过氧化氢的质量一定会发生变化;②水除了原来的,又有水生成,所以水的质量也发生了变化;③二氧化锰是催化剂在反应前后质量和性质都不发生变化.其中发生变化的是①②.
故选C.
点评:了解催化剂的特点是本身在反应前后质量和性质都不发生变化,只是改变反应的速率.

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案
相关题目
归纳与演绎是重要的科学方法,也是常用的化学学习方法.
(1)我们已经学习过实验室制取O2、CO2、H2(Zn和稀硫酸反应)三种气体的反应原理、制取与收集方法.请你归纳出实验室制取气体反应的共同点 (填序号)
①需要加热 ②使用催化剂 ③没有气体参加反应 ④原料为纯净物 ⑤只生成一种气体
(2)下列是实验室常用的仪器
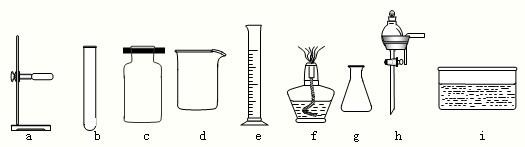
写出仪器名称:a是 ,c是 ;写出d的一种用途 .
(3)化学上可以通过多种反应制得NH3(极易溶于水,密度比空气小),例如
①2NH4Cl(固)+Ca(OH)2(固)
CaCl2+2NH3↑+2H2O
②NH4HCO3(固)
NH3↑+CO2↑+H2O
③CaO(固)+NH3.H2O(浓)═NH3↑+Ca(OH)2
我将选择反应 (只写一个,填序号)作为实验室制取氨气的反应原理.我需要用上面仪器中的 (填序号)来装配氨气发生装置(连接装置已经省略),我采用的收集方法是 .我选择的发生装置还可以用来制取 气体.
(4)某研究小组对用双氧水分解生成水和氧气的实验条件进行探究,完成了以下实验:
①往盛有5ml 5%H2O2溶液的试管中,伸入带火星的木条,木条不复燃.
②往盛有5ml w% H2O2溶液的试管中,加入a g MnO2,伸入带火星的木条,木条复燃.
③往盛有5ml w% H2O2溶液的试管中,加入a g Fe2O3,伸入带火星的木条,木条复燃.
④经检验,②③中反应后试管中仍分别含有a gMnO2和 ag Fe2O3
研究小组还对溶液浓度、催化剂的种类等实验条件进行探究.下表选取了部分实验数据:用足量等体积H2O2溶液制取相同体积O2所需要的时间
(1)我们已经学习过实验室制取O2、CO2、H2(Zn和稀硫酸反应)三种气体的反应原理、制取与收集方法.请你归纳出实验室制取气体反应的共同点
①需要加热 ②使用催化剂 ③没有气体参加反应 ④原料为纯净物 ⑤只生成一种气体
(2)下列是实验室常用的仪器

写出仪器名称:a是
(3)化学上可以通过多种反应制得NH3(极易溶于水,密度比空气小),例如
①2NH4Cl(固)+Ca(OH)2(固)
| ||
②NH4HCO3(固)
| ||
③CaO(固)+NH3.H2O(浓)═NH3↑+Ca(OH)2
我将选择反应
(4)某研究小组对用双氧水分解生成水和氧气的实验条件进行探究,完成了以下实验:
①往盛有5ml 5%H2O2溶液的试管中,伸入带火星的木条,木条不复燃.
②往盛有5ml w% H2O2溶液的试管中,加入a g MnO2,伸入带火星的木条,木条复燃.
③往盛有5ml w% H2O2溶液的试管中,加入a g Fe2O3,伸入带火星的木条,木条复燃.
④经检验,②③中反应后试管中仍分别含有a gMnO2和 ag Fe2O3
| 问题一:请你写出用双氧水和二氧化锰制氧气的化学反应方程式 问题二:MnO2和 Fe2O3在上述反应中的作用是 实验②④中的H2O2的浓度(w%)以 |
| 问题三:从左表中能得到哪些结论?(写出一条结论) |
| 浓度 时间(min) 条件 |
30%H2O2 | 15%H2O2 | 5%H2O2 |
| ag MnO2 | 0.2 | 0.8 | 2.0 |
| ag Fe2O3 | 0.7 | 9.0 | 16.0 |
对氧气的探究

(1)标号仪器的名称为:① ,② .
(2)实验室用过氧化氢和二氧化锰制氧气,反应的化学方程式为 .在甲、乙两套发生装置中,你选择的是 ,另一套装置的错误是 ,容易导致的后果是 .
(3)收集氧气时,可以根据氧气的 和 选择不同的收集方法.要收集一瓶较纯净的氧气,最好选择上图中的 装置.
(4)如果用B装置进行收集,需要验满,方法是:将带火星的木条伸到 ,木条复燃,证明氧气已集满.某同学在锥形瓶内出现大量气泡时,用B装置收集氧气,过一段时间后用带火星的木条伸入瓶口、瓶中、瓶底,都未觅木条复燃,其原因可能是 .
(5)某研究小组对用H2O2分解的实验条件进行探究.他们进行以下试验:
①往盛有5mL 5%H2O2溶液的试管中,伸入带火星的木条,木条不复燃
②往盛有5mL w%H2O2溶液的试管中,加入a g MnO2,伸入带火星的木条,木条复燃
③往盛有5mL w%H2O2溶液的试管中,加入a g Fe2O3,伸入带火星的木条,木条复燃
④经检验,②③中反应的试管中管中仍然有a g MnO2和a g Fe2O3.
研究小组还对溶液浓度、催化剂的种类等实验条件进行了探究.下表选取了部分实验数据.用足量等体积H202溶液制取相同体积02所需的时间
问题:(1)Mn02、Fe203在上述反应中的作用是
问题:(2)实验②、③中H202的浓度(w%)以 为宜.
问题:(3)从上表中能得出哪些结论? .

(1)标号仪器的名称为:①
(2)实验室用过氧化氢和二氧化锰制氧气,反应的化学方程式为
(3)收集氧气时,可以根据氧气的
(4)如果用B装置进行收集,需要验满,方法是:将带火星的木条伸到
(5)某研究小组对用H2O2分解的实验条件进行探究.他们进行以下试验:
①往盛有5mL 5%H2O2溶液的试管中,伸入带火星的木条,木条不复燃
②往盛有5mL w%H2O2溶液的试管中,加入a g MnO2,伸入带火星的木条,木条复燃
③往盛有5mL w%H2O2溶液的试管中,加入a g Fe2O3,伸入带火星的木条,木条复燃
④经检验,②③中反应的试管中管中仍然有a g MnO2和a g Fe2O3.
研究小组还对溶液浓度、催化剂的种类等实验条件进行了探究.下表选取了部分实验数据.用足量等体积H202溶液制取相同体积02所需的时间
| 时间 (min) 浓度 条件 |
30%H2O2 | 15%H2O2 | 5%H2O2 |
| 加入agMnO2 | 0.2 | 0.8 | 2.0 |
| 加入agFe2O3 | 7.0 | 9.0 | 16.0 |
问题:(2)实验②、③中H202的浓度(w%)以
问题:(3)从上表中能得出哪些结论?
归纳与演绎是重要的科学方法,也是常用的化学学习方法.
(1)我们已经学习过实验室制取O2、CO2、H2(Zn和稀硫酸反应)三种气体的反应原理、制取与收集方法.请你归纳出实验室制取气体反应的共同点______(填序号)
①需要加热 ②使用催化剂 ③没有气体参加反应 ④原料为纯净物 ⑤只生成一种气体
(2)下列是实验室常用的仪器

写出仪器名称:a是______,c是______;写出d的一种用途______.
(3)化学上可以通过多种反应制得NH3(极易溶于水,密度比空气小),例如
①2NH4Cl(固)+Ca(OH)2(固) CaCl2+2NH3↑+2H2O
CaCl2+2NH3↑+2H2O
②NH4HCO3(固) NH3↑+CO2↑+H2O
NH3↑+CO2↑+H2O
③CaO(固)+NH3.H2O(浓)═NH3↑+Ca(OH)2
我将选择反应______(只写一个,填序号)作为实验室制取氨气的反应原理.我需要用上面仪器中的______(填序号)来装配氨气发生装置(连接装置已经省略),我采用的收集方法是______.我选择的发生装置还可以用来制取______气体.
(4)某研究小组对用双氧水分解生成水和氧气的实验条件进行探究,完成了以下实验:
①往盛有5ml 5%H2O2溶液的试管中,伸入带火星的木条,木条不复燃.
②往盛有5ml w% H2O2溶液的试管中,加入a g MnO2,伸入带火星的木条,木条复燃.
③往盛有5ml w% H2O2溶液的试管中,加入a g Fe2O3,伸入带火星的木条,木条复燃.
④经检验,②③中反应后试管中仍分别含有a gMnO2和 ag Fe2O3
| 问题一:请你写出用双氧水和二氧化锰制氧气的化学反应方程式 ______ 问题二:MnO2和 Fe2O3在上述反应中的作用是______. 实验②④中的H2O2的浓度(w%)以______为宜. |
| 问题三:从左表中能得到哪些结论?(写出一条结论) |
| 浓度 时间(min) 条件 | 30%H2O2 | 15%H2O2 | 5%H2O2 |
| ag MnO2 | 0.2 | 0.8 | 2.0 |
| ag Fe2O3 | 0.7 | 9.0 | 16.0 |
对氧气的探究

(1)标号仪器的名称为:①______,②______.
(2)实验室用过氧化氢和二氧化锰制氧气,反应的化学方程式为______.在甲、乙两套发生装置中,你选择的是______,另一套装置的错误是______,容易导致的后果是______.
(3)收集氧气时,可以根据氧气的______和______选择不同的收集方法.要收集一瓶较纯净的氧气,最好选择上图中的______装置.
(4)如果用B装置进行收集,需要验满,方法是:将带火星的木条伸到______,木条复燃,证明氧气已集满.某同学在锥形瓶内出现大量气泡时,用B装置收集氧气,过一段时间后用带火星的木条伸入瓶口、瓶中、瓶底,都未觅木条复燃,其原因可能是______.
(5)某研究小组对用H2O2分解的实验条件进行探究.他们进行以下试验:
①往盛有5mL 5%H2O2溶液的试管中,伸入带火星的木条,木条不复燃
②往盛有5mL w%H2O2溶液的试管中,加入a g MnO2,伸入带火星的木条,木条复燃
③往盛有5mL w%H2O2溶液的试管中,加入a g Fe2O3,伸入带火星的木条,木条复燃
④经检验,②③中反应的试管中管中仍然有a g MnO2和a g Fe2O3.
研究小组还对溶液浓度、催化剂的种类等实验条件进行了探究.下表选取了部分实验数据.用足量等体积H202溶液制取相同体积02所需的时间
| 时间 (min) 浓度 条件 | 30%H2O2 | 15%H2O2 | 5%H2O2 |
| 加入agMnO2 | 0.2 | 0.8 | 2.0 |
| 加入agFe2O3 | 7.0 | 9.0 | 16.0 |
问题:(2)实验②、③中H202的浓度(w%)以______为宜.
问题:(3)从上表中能得出哪些结论?______.
