题目内容
(3分) 登山队员常用的能源是氢化钙(CaH2)固体,它和水反应生成氢氧化钙和氢气(CaH2 + 2H2O Ca(OH)2 + 2H2↑),氢气供燃烧之需。现有840 g氢化钙固体,与足量水反应可生成氢气多少克?
80 g。
解析试题分析:找到相关数据,带入化学方程式计算即可。
解:设可制得氢气的质量为x。
CaH2 + 2H2O Ca(OH)2 + 2H2↑
42 4
840 g x 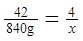
x=80 g
答:可制得氢气80 g。
考点:根据化学方程式计算。
点评:根据化学方程式计算,要注意解题的步骤,设、写、找、列、解、答。

练习册系列答案
相关题目