题目内容
黄铜是一种重要的金属,它是铜和锌的合金,可用来制造机器、电器零件及日常用品.为了测定黄铜样品的组成,取五份样品分别加稀硫酸反应,其实验数据记录如下:

按要求回答下列问题:
(1)根据实验数据分析,从第________份开始,金属已经反应完全了.
(2)列式计算该黄铜样品中金属锌的质量分数.(要求写出计算过程)
答案:4;
提示:
提示:
|
考点:根据化学反应方程式的计算. 专题:综合计算(图像型、表格型、情景型计算题). 分析:(1)第4份加入120 g硫酸生成氢气1.0 g,第5份中又多加了30 g硫酸,但是生成氢气的质量没变,说明锌已经被反应完了;(2)根据生成氢气的质量计算出锌的质量,再用锌的质量除以样品的质量乘以百分之百即可. 解答:解:(1)第4份加入120 g硫酸生成氢气1.0 g,第5份中又多加了30 g硫酸,但是生成氢气的质量没变,说明锌已经被反应完了,所以从第4份开始,金属已经反应完了; (2)解:设40 g样品中含锌的质量为x 所以黄铜样品中锌的质量分数为 答:黄铜样品中锌的质量分数为81.25% 故答案为:(1)4;(2)81.25%. 点评:解答本题关键是要通过图表中数据分析出最多生成氢气1.0 g,再利用方程式计算出锌的质量,再进一步进行计算. |

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目

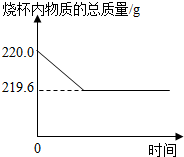 体溶解忽略不计).
体溶解忽略不计).