题目内容
草酸亚铁晶体(FeC2O4•2H2O)是一种浅黄色固体,难溶于水,受热易分解,是生产锂电池的原材料。某化学兴趣小组设计实验验证草酸亚铁晶体热分解的气体产物,并用热重法(TG)确定其分解后所得固体产物的组成。探究过程如下:
【查阅资料】
1.草酸亚铁晶体热分解的气体产物是H2O、CO、CO2。
2.白色的无水CuSO4遇水蒸气会变成蓝色。
3. 浓硫酸具有吸水干燥的性质。
4. 氢氧化钠溶液能与二氧化碳反应生成碳酸钠和水。
【实验设计】

(1)从环保角度考虑,该套实验装置的明显缺陷是 。
(2)可选择以下实验装置中的 (选填“甲”或“乙”)作为虚线中的“热分解装置”。
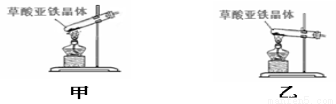
【问题讨论】
(3)实验过程中观察到:B中白色无水CuSO4变成蓝色,C中澄清石灰水变浑浊的反应方程式 (填化学方程式),E中 (填实验现象),则可证明草酸亚铁晶体热分解的气体产物是H2O、CO2、CO。
(4)该兴趣小组进行上述实验时,先点燃热分解装置中的酒精灯,一段时间后再点燃E处的酒精灯,原因是 。
(5)若通过F装置中澄清石灰水变浑浊来证明草酸亚铁晶体热分解的气体产物中有CO,则需在C和D装置之间增加盛有足量的浓氢氧化钠溶液的洗气瓶,其作用是 。
【数据分析】
(6)称取3.60g草酸亚铁晶体(FeC2O4•2H2O,相对分子质量是180)用热重法对其进行热分解,得到剩余固体的质量随温度变化的曲线如图所示,请分析该图回答下列问题:
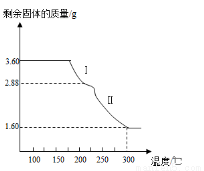
①过程Ⅰ发生反应的化学方程式为 。
②300℃时剩余固体只有一种且是铁的氧化物, 试通过计算确定该氧化物的化学式或名称 。
请写出计算过程:
 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案汽油主要组成元素是碳和氢,发动机中汽油与空气参与了一系列反应.学习小组为了探究某汽车所排放气体的成分,进行如下实验.
【猜想】
该气体可能含有 、 及少量的CO、NO和NO2等.你猜想含有这些气体的依据是 。
【查阅资料】
①NO是无色无味、难溶于水的有毒气体,NO2是红棕色、有刺激性气味的有毒气体。
②一氧化氮遇到氧气发生反应:2NO+O2═2NO2;
二氧化氮通入水中发生反应:3NO2+H2O═2HNO3+NO.
③CO和NO均可使新鲜血液变质而使颜色变暗.
【实验探究】
实验步骤 | 实验现象 | 实验结论及化学方程式 |
(1)用球胆收集汽车排出气体 | -------- | -------- |
(2)闻该气体气味 | 有刺激性气味 | 该气体中可能含有 |
(3)将该气体通入足量澄清石灰水中 | 有白色沉淀生成 | 该气体中一定含有 ,生成白色沉淀的化学方程式是 。 |
(4) | C中新鲜血液颜色变暗;D中有红棕色气体产生。 | 该气体中,除了(3)所确定的成分外,下列有关其余成分的说法一定不正确的是 ①只含NO ②只含NO2 ③只含CO ④含NO和NO2 ⑤含CO和NO2 ⑥含CO和NO ⑦含CO、NO和NO2 |
(5)将(4)中C导出的气体通入 | 观察到 . | 该气体中一定含有CO |
【计算】将汽车排放的废气经过处理只含二氧化碳和一氧化碳,若用10g这种气体通过足量的氧化铁,高温一段时间后收集到12.4g气体,则10g气体中二氧化碳的质量为 。
空气中氧气含量测定的再认识。
【实验回顾】
图1是实验室用红磷燃烧来粗略测定空气中氧气含量的装置。
(1)写出红磷燃烧的符号表达式 。
(2)实验原理:由于红磷燃烧消耗空气中的氧气,使瓶内气体的 减小,烧杯中水倒吸到集气瓶。
【问题提出】
有实验资料表明:燃烧过程中当氧气体积分数低于7% 时,红磷就无法继续燃烧,因此通过上述实验,测定结果与理论值往往相差较大。

【实验改进】
Ⅰ. 甲同学根据铁在空气中生锈的原理设计图2实验装置,再次测定空气中氧气含量(装置中装铁粉的纸袋浸有浓食盐水,会加速铁生锈)。
Ⅱ. 乙同学经过思考,在图2的基础上设计了图3实验装置,实验测得实验数据如下表:
时间/h | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
压强/KP | 101.6 | 89.7 | 85.4 | 83.3 | 82.2 | 81.] | 81.2 | 81.2 | 81.2 |
【交流表达】
(1)根据表中数据计算,改进后测得空气中氧气的体积分数是 (结果精确到0.1%)。
(2)从实验原理角度分析,图2的实验结果比图1准确度更髙的主要原因是: 。
【实验反思】
许多同学用改进前图1装置得出的结论却也与理论值相差不大,其主要原因是:





