��Ŀ����
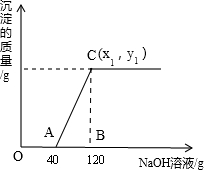
�������MgCl2�Ļ����Һ��100g��������Һ����μ���������������Ϊ10%��NaOH��Һ�����ɵij���������NaOH��Һ������ϵ����ͼ��ʾ����HCl�ڻ����Һ����������Ϊ3.65%����

��1��A����Һ�����ʻ�ѧʽΪ ��
��2�������ᷴӦ��������������Ϊ g��
��3��ǡ�ó�����ȫʱ��C��������Һ�����ʵ����������Ƕ���?�������ȷ��0.1% ��д��������̣�
NaCl��MgCl2��40g��8.2%
��������
�����������1����ͼ�����ݿ�֪����ʼ��������������Һ��û�г������ɣ�˵�������������������ᷴӦ����MgCl2��δ��Ӧ����A��ʱ����������������ǡ����ȫ��Ӧ�������Ȼ��ƺ�ˮ����A����Һ�����ʻ�ѧʽΪ���ɵ�NaCl��δ��Ӧ��MgCl2��
��2��������A��ʱ����������������ǡ����ȫ��Ӧ���ʿɸ�����������������ö��߷�Ӧ�Ļ�ѧ����ʽ��������μӷ�Ӧ���������Ƶ�����
�������ᷴӦ������������Һ������Ϊx
NaOH + HCl =" NaCl" + H2O
40 36.5
x��10% 100g��3.65%
40:36.5=(x��10%):(100g��3.65%)
��ã�x=40g
�������ᷴӦ��������������Ϊ40g��
��3�����������֪��MgCl2���������Ʒ�Ӧ������������þ�������Ȼ��ƣ����ͼʾ��֪����Ӧ��C��ʱ������ǡ����ȫ��Ӧ����Һ�е�����Ϊ�Ȼ��ƣ����Ȼ��������������֣��������������ᷴӦ���ɵ��Ȼ��ƣ�MgCl2���������Ʒ�Ӧ���ɵ��Ȼ��ƣ������ݡ�������������=  ��100%�����㼴�ɡ�
��100%�����㼴�ɡ�
���ͼʾ���ݿ�֪����MgCl2��Ӧ������������Һ������Ϊ120g-40g=80g��
��MgCl2���������Ʒ�Ӧ���ɵ��Ȼ��Ƶ�����Ϊy�����ɵ�������þ����������Ϊm
2NaOH + MgCl2 =" 2NaCl" + Mg(OH)2��
80 117 58
80g��10% y m
80:117=(80g��10%):y
��ã�y=11.7g
80:58=(80g��10%):m
��ã�m=5.8g
���������������ᷴӦ���ɵ��Ȼ��Ƶ�����Ϊz��
HCl + NaOH = NaCl + H2O
36.5 58.5
100g��3.65% z
36.5��58.5=(100g��3.65%)��z
��ã�z=5.85g
���ԣ�C��������Һ�����ʵ���������=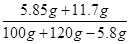 ��100%=��8.2%��
��100%=��8.2%��
���㣺�ᡢ��εĻ�ѧ���ʣ���д��ѧ����ʽ�����ݻ�ѧ��Ӧ����ʽ�ļ���
�����������ǹ��ڻ�ѧ����ʽ���������������ļ����⣬Ҫ��ѧ���н�ǿ��ʶͼ���������ݷ�������������Ĺؼ��Ǹ���ͼ���ҳ�ǡ����ȫ��Ӧʱ�����ʵ���������������صĻ�ѧ��Ӧ����ʽ����������֪����δ֪��Ӧ�������������㼴�ɣ����ڷ�Ӧ�������Ҫע������������������֣�������Ӧ���ã���

 â���̸������Ծ�ϵ�д�
â���̸������Ծ�ϵ�д�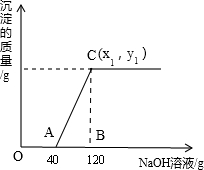
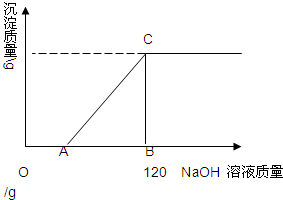 �������MgCl2�Ļ����Һ��100g��������Һ����μ���������������Ϊ10%��NaOH��Һ�����ɵij���������NaOH��Һ������ϵ��ͼ��ʾ����HCl�ڻ����Һ����������Ϊ3.65%����
�������MgCl2�Ļ����Һ��100g��������Һ����μ���������������Ϊ10%��NaOH��Һ�����ɵij���������NaOH��Һ������ϵ��ͼ��ʾ����HCl�ڻ����Һ����������Ϊ3.65%����
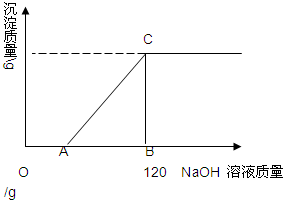 �������MgCl2�Ļ����Һ��100g��������Һ����μ���������������Ϊ10%��NaOH��Һ�����ɵij���������NaOH��Һ������ϵ��ͼ��ʾ����HCl�ڻ����Һ����������Ϊ3.65%����
�������MgCl2�Ļ����Һ��100g��������Һ����μ���������������Ϊ10%��NaOH��Һ�����ɵij���������NaOH��Һ������ϵ��ͼ��ʾ����HCl�ڻ����Һ����������Ϊ3.65%����