题目内容
现有Na2CO3和Na2SO4的固体混合物共18g,将它放入98g20%的H2SO4溶液中,充分反应后溶液呈酸性;向此酸性溶液中再逐滴加入84g10%的Na2CO3溶液,恰好完全反应.计算所得溶液中溶质的质量分数.(计算结果精确到0.1%)
解:设参加反应的Na2CO3的质量为x,生成Na2SO4的质量为y,生成CO2的质量为z.
Na2CO3+H2SO4=Na2SO4+H2O+CO2↑
106 98 142 44
x 98g×20% y z
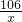 =
= =
= =
=
x=21.2g y=28.4g z=8.8g
原固体混合物中Na2CO3质量为:21.2g-84g×10%=12.8g
Na2SO4总质量为:28.4g+(18g-12.8g)=33.6g
反应后所得溶液中硫酸钠的质量分数为: ×100%=17.6%
×100%=17.6%
答:反应后所得溶液中硫酸钠的质量分数为17.6%.
分析:固体混合物溶于稀硫酸形成硫酸钠溶液,充分反应后溶液呈酸性表明硫酸过量,过量的硫酸与继续滴入的碳酸钠溶液恰好完全反应,因此反应后所得溶液为硫酸钠溶液,其中硫酸钠由两次所加碳酸钠与硫酸恰好完全反应生成硫酸钠与混合物中所含硫酸钠所构成.要计算所得溶液的质量分数,需要利用反应的化学方程式由所用硫酸的质量计算参加反应的碳酸钠的质量、生成硫酸钠的质量及放出二氧化碳质量,以求得混合物中硫酸钠的质量及反应后所得溶液质量.
点评:根据质量守恒定律,反应后所得溶液的质量=固体混合物的质量+所加稀硫酸的质量+所滴加碳酸钠溶液的质量-放出二氧化碳的总质量.
Na2CO3+H2SO4=Na2SO4+H2O+CO2↑
106 98 142 44
x 98g×20% y z
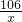 =
= =
= =
=
x=21.2g y=28.4g z=8.8g
原固体混合物中Na2CO3质量为:21.2g-84g×10%=12.8g
Na2SO4总质量为:28.4g+(18g-12.8g)=33.6g
反应后所得溶液中硫酸钠的质量分数为:
 ×100%=17.6%
×100%=17.6%答:反应后所得溶液中硫酸钠的质量分数为17.6%.
分析:固体混合物溶于稀硫酸形成硫酸钠溶液,充分反应后溶液呈酸性表明硫酸过量,过量的硫酸与继续滴入的碳酸钠溶液恰好完全反应,因此反应后所得溶液为硫酸钠溶液,其中硫酸钠由两次所加碳酸钠与硫酸恰好完全反应生成硫酸钠与混合物中所含硫酸钠所构成.要计算所得溶液的质量分数,需要利用反应的化学方程式由所用硫酸的质量计算参加反应的碳酸钠的质量、生成硫酸钠的质量及放出二氧化碳质量,以求得混合物中硫酸钠的质量及反应后所得溶液质量.
点评:根据质量守恒定律,反应后所得溶液的质量=固体混合物的质量+所加稀硫酸的质量+所滴加碳酸钠溶液的质量-放出二氧化碳的总质量.

练习册系列答案
相关题目
![]()
现有由海水晒得的粗盐,其中含有CaCl2和MgCl2两种杂质。某活动小组将粗盐溶于水后设计了两种除去粗盐中杂质的方法,所用到的试剂均为A、NaOH溶液;B、Na2CO3溶液;C、稀盐酸,除杂的两种方法如下:
请回答:
(1)方法一的滤液③中含有的溶质分别为 (用化学式表示)
(2)方法二的滤液③中含有的溶质分别为 (用化学式表示)
(3)根据两种固体M、N的成分分析哪一种方法合理 。

 (2011?盂县一模)现有铁、氧化铁、稀盐酸、氢氧化钙溶液、碳酸钠溶液五种物质,存在如图所示的相互反应和转化关系,图中“-”表示两端的物质间可以发生化学反应,“→”表示物质间存在相应的转化关系,回答下列问题:
(2011?盂县一模)现有铁、氧化铁、稀盐酸、氢氧化钙溶液、碳酸钠溶液五种物质,存在如图所示的相互反应和转化关系,图中“-”表示两端的物质间可以发生化学反应,“→”表示物质间存在相应的转化关系,回答下列问题:
