题目内容
某质量的锌粒与100g稀盐酸溶液恰好完全反应,产生氢气0.4g.锌粒的质量为
13
13
g,稀盐酸的质量分数为14.6%
14.6%
,发生反应的化学方程式Zn+2HCl═ZnCl2+H2↑
Zn+2HCl═ZnCl2+H2↑
,反应类型是置换反应
置换反应
.分析:依据锌粒与盐酸的反应方程式依据氢气的质量可求出锌粒的质量以及反应的氯化氢的质量,进而依据盐酸的质量求出盐酸的质量分数,依据反应物生成物的种类可判断反应的类型;
解答:解:设参加反应的氯化氢的质量为x,锌的质量为y
Zn+2HCl═ZnCl2+H2↑
65 73 2
y x 0.4g
=
=
解得 x=14.6g
y=13g
盐酸的质量分数为:
×100%=14.6%
锌与稀盐酸的反应反应物是单质与化合物生成物是另一种单质与化合物,所以该反应应该属于置换反应;
故答案为:13;14.6%;Zn+2HCl═ZnCl2+H2↑;置换反应;
Zn+2HCl═ZnCl2+H2↑
65 73 2
y x 0.4g
| 65 |
| y |
| 73 |
| x |
| 2 |
| 0.4g |
解得 x=14.6g
y=13g
盐酸的质量分数为:
| 14.6g |
| 100g |
锌与稀盐酸的反应反应物是单质与化合物生成物是另一种单质与化合物,所以该反应应该属于置换反应;
故答案为:13;14.6%;Zn+2HCl═ZnCl2+H2↑;置换反应;
点评:本题考查了根据化学方程式的计算,完成此题,可以依据反应的化学方程式进行.

练习册系列答案
相关题目
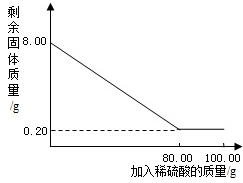 在通常状况下,氢气是一种无色、无味的气体,难溶于水,密度比空气小.实验室常用锌粒和稀硫酸反应制取氢气:Zn+H2SO4═ZnSO4+H2↑.为了得到0.20s氢气,某同学用质量为8.00g含有杂质的锌粒与100.00g过量的稀硫酸反应,该同学测得的有关实验数据如下图函数关系.(假定杂质不溶于水,也不参加反应.)
在通常状况下,氢气是一种无色、无味的气体,难溶于水,密度比空气小.实验室常用锌粒和稀硫酸反应制取氢气:Zn+H2SO4═ZnSO4+H2↑.为了得到0.20s氢气,某同学用质量为8.00g含有杂质的锌粒与100.00g过量的稀硫酸反应,该同学测得的有关实验数据如下图函数关系.(假定杂质不溶于水,也不参加反应.) 在通常状况下,氢气是一种无色、无味的气体,难溶于水,密度比空气小.实验室常用锌粒和稀硫酸反应制取氢气:Zn+H2SO4═ZnSO4+H2↑.为了得到0.20s氢气,某同学用质量为8.00g含有杂质的锌粒与100.00g过量的稀硫酸反应,该同学测得的有关实验数据如下图函数关系.(假定杂质不溶于水,也不参加反应.)
在通常状况下,氢气是一种无色、无味的气体,难溶于水,密度比空气小.实验室常用锌粒和稀硫酸反应制取氢气:Zn+H2SO4═ZnSO4+H2↑.为了得到0.20s氢气,某同学用质量为8.00g含有杂质的锌粒与100.00g过量的稀硫酸反应,该同学测得的有关实验数据如下图函数关系.(假定杂质不溶于水,也不参加反应.)