题目内容
 根据如图硝酸钾和氯化钠的溶解度曲线,有关叙述正确的是( )
根据如图硝酸钾和氯化钠的溶解度曲线,有关叙述正确的是( )分析:根据溶解度曲线的意义:比较溶解度的大小,溶解度随温度变化的情况,将饱和溶液改变温度时溶液的溶质质量分数变化,由溶解度判断溶液是否饱和等.
解答:解:A、由溶解度曲线的意义可知,硝酸钾和氯化钠的溶解度曲线相交于一点,说明了交点时的温度下,溶解度相等,故A错误;
B、由溶解度曲线的意义可知,随温度的升高,氯化钠的溶解度略有增加,故B错误;
C、由溶解度曲线的意义可知,随温度的升高,硝酸钾的溶解度增加,10℃硝酸钾饱和溶液,温度升高到20℃,溶液中溶质的质量不变,其溶液的溶质质量分数不变,故C错误;
D、由溶解度曲线的意义可知,30℃时,氯化钠的溶解度小于40g,所以,30℃时,40g氯化钠加入100g水中,充分搅拌后,可得到饱和溶液,故D正确.
故选D.
B、由溶解度曲线的意义可知,随温度的升高,氯化钠的溶解度略有增加,故B错误;
C、由溶解度曲线的意义可知,随温度的升高,硝酸钾的溶解度增加,10℃硝酸钾饱和溶液,温度升高到20℃,溶液中溶质的质量不变,其溶液的溶质质量分数不变,故C错误;
D、由溶解度曲线的意义可知,30℃时,氯化钠的溶解度小于40g,所以,30℃时,40g氯化钠加入100g水中,充分搅拌后,可得到饱和溶液,故D正确.
故选D.
点评:本题难度不是很大,主要考查了根据固体物质的溶解度曲线解决相关的问题,从而培养学生对固体溶解度曲线意义的理解和应用.

练习册系列答案
 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案
相关题目
 28、如图为氯化钠和硝酸钾固体的溶解度曲线.
28、如图为氯化钠和硝酸钾固体的溶解度曲线.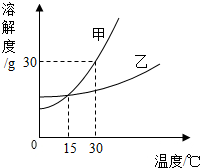 (2006?淄博)以下是同学们在学习溶液知识时实验报告中的部分内容,分析后请回答:
(2006?淄博)以下是同学们在学习溶液知识时实验报告中的部分内容,分析后请回答: 如图表示硝酸钾和氯化钠的溶解度曲线.请根据图回答下列问题:
如图表示硝酸钾和氯化钠的溶解度曲线.请根据图回答下列问题: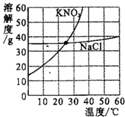 根据如图硝酸钾和氯化钠的溶解度曲线,有关叙述正确的是
根据如图硝酸钾和氯化钠的溶解度曲线,有关叙述正确的是