题目内容
12.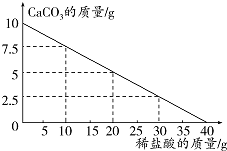 向10g碳酸钙中不断加入稀盐酸,其质量变化如图所示.请计算:
向10g碳酸钙中不断加入稀盐酸,其质量变化如图所示.请计算:(1)当10g碳酸钙恰好完全反应时,消耗稀盐酸的质量为40g.
(2)反应所得溶液中CaCl2的质量分数(写出计算过程,结果精确到0.1%).
分析 (1)由图象可知:当CaCO3质量为0时,即为盐酸与CaCO3恰好完全反应的时刻,此时所用稀盐酸的量即是所消耗的稀盐酸,故10g CaCO3完全反应时,所加稀盐酸的质量为40g.
(2)根据碳酸钙与盐酸反应的化学方程式,由碳酸钙的质量科求出生成的氯化钙、二氧化碳的质量,再根据溶质的质量分数计算公式计算.
解答 解:(1)如图象所示:当10gCaCO3恰好完全反应时,所加稀盐酸的质量40g;
(2)设生成氯化钙的质量为x,生成二氧化碳的质量为y
2HCl+CaCO3=CaCl2+H2O+CO2↑
100 111 44
10g x y
$\frac{100}{10g}=\frac{111}{x}=\frac{44}{y}$
x=11.1g
y=4.4g
恰好完全反应后所得溶液中的溶质质量分数为:$\frac{11.1g}{10g+40g-4.4g}×$100%≈24.3%
答案:
(1)40;
(2)恰好完全反应后所得溶液中的溶质质量分数为:24.3%.
点评 本题考查内容简单注重基础,熟练掌握有关化学方程式的计算,以及溶质质量分数的计算是解题关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.科学家最新发现,通过简单的化学反应,可以将树木纤维素转变成超级储能装置,如图是该反应的微观示意图,下列说法错误的是( )
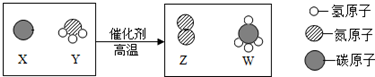

| A. | 化学反应前后原子的种类、数目、质量均保持不变 | |
| B. | W物质中碳元素的质量分数为75% | |
| C. | 参加反应的X、Y两物质的粒子个数比为3:4 | |
| D. | 反应前后各元素的化合价均不变 |
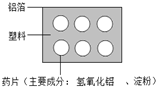
7. 某化学兴趣小组利用如图所示的改进装置测定空气中氧气的体积分数.关于该实验有下列说法:
某化学兴趣小组利用如图所示的改进装置测定空气中氧气的体积分数.关于该实验有下列说法:
①白磷燃烧会产生大量的白雾;
②白磷不足,会使测定结果偏小;
③实验中注射器活塞先向右移动,后向左移动;
④若注射器活塞最终停在10mL刻度处,说明氧气体积分数约为$\frac{1}{5}$;
⑤胶头滴管与注射器中的水,作用相同.
其中正确的是( )
 某化学兴趣小组利用如图所示的改进装置测定空气中氧气的体积分数.关于该实验有下列说法:
某化学兴趣小组利用如图所示的改进装置测定空气中氧气的体积分数.关于该实验有下列说法:①白磷燃烧会产生大量的白雾;
②白磷不足,会使测定结果偏小;
③实验中注射器活塞先向右移动,后向左移动;
④若注射器活塞最终停在10mL刻度处,说明氧气体积分数约为$\frac{1}{5}$;
⑤胶头滴管与注射器中的水,作用相同.
其中正确的是( )
| A. | ①②③④ | B. | ②③④⑤ | C. | ②③④ | D. | ③④⑤ |
17.下列图示的实验操作不正确的是( )
| A. |  用橡皮塞塞住试管 | B. |  除去CO中的HCl | ||
| C. |  稀释浓硫酸 | D. |  研碎固体并闻气味 |
1.常用的“灭火弹”里装有液态四氯化碳,使用时,液态四氯化碳迅速转化为气态并覆盖在火焰上.据此推测,四氯化碳可能具有的化学性质是( )
| A. | 气态时密度比空气大 | B. | 沸点较低,容易气化 | ||
| C. | 不支持燃烧 | D. | 可燃性 |
 《奔跑吧 兄弟》是一档热播的娱乐节目,其中蕴含着许多化学知识.
《奔跑吧 兄弟》是一档热播的娱乐节目,其中蕴含着许多化学知识.
 右图中A~G均是初中化学常见物质,它们之间的转化或相互反应关系均为初中常见反应,其中G属于单质,且被称为最理想能源,其余均为化合物,B是胃酸的主要成分,B和C物质类别相同,D是常用的食品干燥剂,E溶于水所得溶液的pH大于7.图中“-”表示两端的物质能发生化学反应,“→”表示物质间存在转化关系,反应条件、部分反应物和生成物已略去.
右图中A~G均是初中化学常见物质,它们之间的转化或相互反应关系均为初中常见反应,其中G属于单质,且被称为最理想能源,其余均为化合物,B是胃酸的主要成分,B和C物质类别相同,D是常用的食品干燥剂,E溶于水所得溶液的pH大于7.图中“-”表示两端的物质能发生化学反应,“→”表示物质间存在转化关系,反应条件、部分反应物和生成物已略去.