题目内容
选择恰当的试剂或方法除去括号内的杂质.
(1)CaO(CaCO3) .
(2)Cu(Fe) .
(3)NaCl(CaCl2) .
(4)NaOH溶液(Na2CO3) .
(1)CaO(CaCO3)
(2)Cu(Fe)
(3)NaCl(CaCl2)
(4)NaOH溶液(Na2CO3)
考点:物质除杂或净化的探究,金属的化学性质,盐的化学性质
专题:物质的分离、除杂、提纯与共存问题
分析:根据除杂的原则:不增加新的杂质,不减少所需物质的量,转化产物易于分离,再结合具体物质利用两者的性质选择合适试剂和方法.
解答:解:(1)碳酸钙在高温煅烧的条件下,能分解成氧化钙和二氧化碳气体,故答案为:高温煅烧
(2)铜与铁的金属活动性有差异,铁排在氢之前,能与稀酸反应生成氢气和亚铁盐,而铜排在氢之后,不与稀酸反应,故答案为:稀盐酸(本题目的混不清楚,如果是合金方式则只能采用化学方法,如果简单的是铜粉和铁粉混在一起,则可以用磁铁)
(3)氯化钙与氯化钠的差异在金属阳离子不同,只需将钙离子转化为沉淀碳酸根,故答案为:碳酸钠溶液.
(4)NaOH溶液中的碳酸钠可加入适量氢氧化钙溶液即澄清的石灰水将碳酸根离子转化成沉淀除去,故答案:澄清的石灰水.
(2)铜与铁的金属活动性有差异,铁排在氢之前,能与稀酸反应生成氢气和亚铁盐,而铜排在氢之后,不与稀酸反应,故答案为:稀盐酸(本题目的混不清楚,如果是合金方式则只能采用化学方法,如果简单的是铜粉和铁粉混在一起,则可以用磁铁)
(3)氯化钙与氯化钠的差异在金属阳离子不同,只需将钙离子转化为沉淀碳酸根,故答案为:碳酸钠溶液.
(4)NaOH溶液中的碳酸钠可加入适量氢氧化钙溶液即澄清的石灰水将碳酸根离子转化成沉淀除去,故答案:澄清的石灰水.
点评:本题考查了除杂的方法和试剂的选择,运用物质的具体性质解题,也是学生需要掌握的基础知识.

练习册系列答案
相关题目
据报道,2007年9月澳门爱国人士何鸿燊出巨资购得流落海外的圆明园稀世生肖铜马首,并捐献给国家.铜铸的马首,是由含一定比例金、银、锡、锌的铜合金铸造的.铜合金属于( )
| A、金属材料 | B、无机非金属材料 |
| C、合成材料 | D、复合材料 |
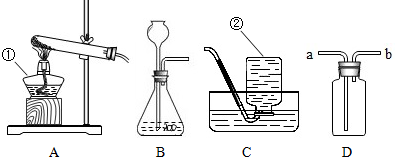
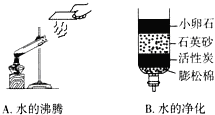 水是重要的自然资源.
水是重要的自然资源.