题目内容
50g
镁、锌、铁的混合物与足量的稀硫酸反应,得到的混合溶液蒸发后得到218g固体(已换算成无水硫酸盐).则反应产生的氢气质量是[
]|
A .2g |
B .3g |
C .3.5g |
D .4.5g |
答案:C
解析:
解析:
|
镁、锌、铁都可以与硫酸反应,生成对应的硫酸盐和氢气,因不知道某一金属或某一种生成物的质量,因此只能将三个反应综合起来考虑,即三种金属置换出硫酸中的氢元素后,生成了 218g无水硫酸盐,因此,硫酸盐中硫酸根离子的质量就是218g-50g=168g,根据质量守恒以及硫酸中硫酸根离子的质量分数可求出硫酸质量为:
即 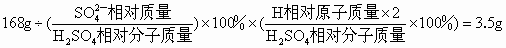 本题综合考查了金属与酸反应、质量守恒定律以及化学式的计算等知识.
本题综合考查了金属与酸反应、质量守恒定律以及化学式的计算等知识. |

练习册系列答案
相关题目
