题目内容
2.20℃时,将等质量a、b两种固体,分别加入到盛有l00g水的烧杯中,充分搅拌后现象如图甲,升温到50℃时,现象如图乙,a、b两种固体的溶解度曲线如图丙.下列说法中正确的是( )
| A. | 图甲a、b溶液中的溶质质量相等 | B. | 图乙a、b溶液一定是不饱和溶液 | ||
| C. | 图丙M表示a物质的溶解度曲线 | D. | 30℃时a、b溶液溶质质量分数不相等 |
分析 A、根据图甲a中有剩余固体,b中无剩余固体解答;
B、图乙无溶质剩余,无法判断是否是饱和溶液;
C、图甲中20℃时,将等质量的甲、乙两种固体物质(不含结晶水),分别加入到盛有100g水的烧杯中,甲有固体剩余,说明甲的溶解度小于乙,结合图3完成解答;
D、根据图3可知两种物质的溶解度都随温度升高而增大,因此30℃时,甲乙的溶解度都比20℃时大,且30℃时两物质的溶解度相等进行解答.
解答 解:A、20℃时,将等质量的a、b两种固体,分别加入到盛有lO0g水的烧杯中,充分搅拌后,a中有剩余固体,b中无剩余固体,溶液中溶质的质量分数a应小于b,故A错误;
B、由于图乙无溶质剩余,无法判断是否是饱和溶液,故B错误;
C、根据图甲中信息可以知道20℃时a的溶解度小于b的溶解度,而图3中在20℃时,N曲线的溶解度大于M曲线的溶解度,故M表示的是a物质的溶解度曲线,故正确;
D、根据图丙可知两种物质的溶解度都随温度升高而增大,因此30℃时,a、b的溶解度都比20℃时大,且30℃时两物质的溶解度相等,当a中的物质完全溶解时,溶质的质量分数就会相等,故D不正确.
故选C.
点评 本题首先要熟记和理解固体溶解度曲线及其使用,溶质质量分数及其有关计算,饱和溶液和不饱和溶液的概念及其相互转变方法,以及物质的溶解和结晶的方法等相关知识;然后,根据所给的问题情景或图表信息,结合所学的相关知识和技能按照题目的要求,认真地进行选择或解答即可.

练习册系列答案
相关题目
10.通过如表实验操作和现象能得出相应结论的是( )
| 实验操作 | 现象 | 结论 | |
| A | 向收集满CO2的软塑料瓶中加入约$\frac{1}{3}$体积滴有石蕊试液的水,旋紧瓶盖,振荡 | 塑料瓶变瘪,溶液变红 | CO2能与石蕊试液变红 |
| B | 向浸没在热水中的白磷通氧气 | 白磷燃烧 | 燃烧需要氧参与 |
| C | 在无色溶液中滴加氯化钡溶液 | 有白色沉淀生成 | 溶液中一定含有SO42- |
| D | 向盛有氢氧化钡溶液的烧杯中滴加稀盐酸 | 无明显现象 | 两者不发生反应 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
7. 化学兴趣小组的同学发现实验台上一瓶标签破损的无色溶液(标签如图).他们提出可能是Na2SO4、NaHCO3、Na2CO3溶液中的一种,于是决定对这瓶溶液进行实验探究.查阅资料:三种物质溶液在常温下的pH 如表
化学兴趣小组的同学发现实验台上一瓶标签破损的无色溶液(标签如图).他们提出可能是Na2SO4、NaHCO3、Na2CO3溶液中的一种,于是决定对这瓶溶液进行实验探究.查阅资料:三种物质溶液在常温下的pH 如表
(1)小新同学认为该溶液不可能的是NaHCO3,理由是化学式中Na的右下角没有2.
(2)标签破损的原因标签破损的原因倾倒液体时,标签没有向着手心.
(3)为确定其成分,小新同学设计如下方案进行探究
(4)小芳认为可以设计更简单的实验方案,该方案是:试管取少量无色溶液,加入酚酞,若溶液变红,则原溶液是碳酸钠溶液 (写出实验步骤、现象及结论).
 化学兴趣小组的同学发现实验台上一瓶标签破损的无色溶液(标签如图).他们提出可能是Na2SO4、NaHCO3、Na2CO3溶液中的一种,于是决定对这瓶溶液进行实验探究.查阅资料:三种物质溶液在常温下的pH 如表
化学兴趣小组的同学发现实验台上一瓶标签破损的无色溶液(标签如图).他们提出可能是Na2SO4、NaHCO3、Na2CO3溶液中的一种,于是决定对这瓶溶液进行实验探究.查阅资料:三种物质溶液在常温下的pH 如表 | 溶液 | Na2SO4 | NaHCO3 | Na2CO3 |
| pH | pH=7 | pH>7 | pH>7 |
(2)标签破损的原因标签破损的原因倾倒液体时,标签没有向着手心.
(3)为确定其成分,小新同学设计如下方案进行探究
| 实验步骤 | 现象 | 结论 |
| 取该溶液少许于试管中,滴加过量的BaCl2溶液,振荡. | ①产生白色沉淀 | 则该溶液是Na2CO3溶液 |
| 过滤,向滤渣滴加稀盐酸. | ②产生气泡 |
11.CO2在高温下能与木炭反应生成CO.为验证该反应,某课外兴趣小组设计了一套实验装置,装置图如图所示(夹持装置及加热部分未画出):

(1)根据装置图,填写如表:
(2)D处要增加的仪器名称是酒精灯.
(3)写出CO2在高温下与木炭反应生成CO的化学方程式CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO.
(4)验证CO的方法是点燃气体,火焰呈蓝色,再用内壁附着有澄清石灰水的烧杯罩在火焰上,烧杯内壁的石灰水变浑浊.

(1)根据装置图,填写如表:
| 仪器标号 | 仪器中所加物质 | 作 用 |
| A | 石灰石,稀盐酸 | 石灰石与盐酸作用产生CO2 |
| B | 饱和碳酸氢钠溶液(与CO2不反应) | 除去CO2中的HCl气体 |
| C | 浓硫酸 | 干燥CO2气体 |
| D | 干燥的木炭粉 | 与CO2反应生成CO |
| E | 澄清石灰水(或Na0H溶液) | 吸收未反应的CO2 |
(3)写出CO2在高温下与木炭反应生成CO的化学方程式CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO.
(4)验证CO的方法是点燃气体,火焰呈蓝色,再用内壁附着有澄清石灰水的烧杯罩在火焰上,烧杯内壁的石灰水变浑浊.
12.2015年11月2日,C919大型客机首架机正式下线.制造大飞机使用了大量的铝、铁、铜.小组同学对三种金属进行了如下探究:
【实验】
【分析】(1)实验时,需先用砂纸打磨金属片,其目的是除去金属表面的氧化膜,利于反应.
(2)如果要验证铝、铁、铜三种金属活动性强弱,从优化实验的角度考虑,只需利用上述实验中的BE(用实验编号填空)两组实验就能达到目的.
(3)将打磨后的铝片放入稀硫酸中,开始反应很慢,然后试管逐渐变热,反应逐渐加快.一段时间后,反应速率变慢,最后停止产生气泡.请结合所学知识,解释产生该现象的原因铝易被空气中的氧气氧化,在铝条表面生成一层致密的氧化物保护膜铝易被空气中的氧气氧化,在铝条表面生成一层致密的氧化物保护膜.将铝条放入稀盐酸中,稀盐酸与铝条表面的氧化铝反应,所以气泡较少.随着氧化铝的减少,铝与盐酸接触面积增大,气泡逐渐增加并达到反应最快.后来盐酸的质量分数越来越小,反应速率减慢.直至停止.
【拓展】将一定质量的锌粉加入含硝酸铝、硝酸铜和硝酸银的溶液中,充分反应后过滤,然后分别向滤液、滤渣中加入稀盐酸,均无明显现象,则滤液中存在的阳离子可能是Al3+、Zn2+或Al3+、Zn2+、Cu2+或Al3+、Zn2+、Cu、Ag+(用离子符号表示所有可能存在的情况).
【实验】
| 实验 | 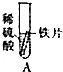 | 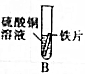 | 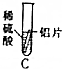 | 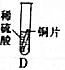 | 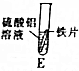 |
| 现象 | 有气泡产生,产生气泡较慢 | 铁片上有红色物质附着,溶液变成浅绿色 | 有气泡产生,产生气泡较快 | 无现象 | 无气泡产生无明显现象 |
(2)如果要验证铝、铁、铜三种金属活动性强弱,从优化实验的角度考虑,只需利用上述实验中的BE(用实验编号填空)两组实验就能达到目的.
(3)将打磨后的铝片放入稀硫酸中,开始反应很慢,然后试管逐渐变热,反应逐渐加快.一段时间后,反应速率变慢,最后停止产生气泡.请结合所学知识,解释产生该现象的原因铝易被空气中的氧气氧化,在铝条表面生成一层致密的氧化物保护膜铝易被空气中的氧气氧化,在铝条表面生成一层致密的氧化物保护膜.将铝条放入稀盐酸中,稀盐酸与铝条表面的氧化铝反应,所以气泡较少.随着氧化铝的减少,铝与盐酸接触面积增大,气泡逐渐增加并达到反应最快.后来盐酸的质量分数越来越小,反应速率减慢.直至停止.
【拓展】将一定质量的锌粉加入含硝酸铝、硝酸铜和硝酸银的溶液中,充分反应后过滤,然后分别向滤液、滤渣中加入稀盐酸,均无明显现象,则滤液中存在的阳离子可能是Al3+、Zn2+或Al3+、Zn2+、Cu2+或Al3+、Zn2+、Cu、Ag+(用离子符号表示所有可能存在的情况).

 ,则x=11
,则x=11
 如图是某校初三(二)班阳光小组的同学们设计的探究铁制品锈蚀条件下的实验装置图,请你一起参与探究,并回答相关问题.
如图是某校初三(二)班阳光小组的同学们设计的探究铁制品锈蚀条件下的实验装置图,请你一起参与探究,并回答相关问题.