题目内容
实验室用锌和稀硫酸反应制取氢气,现在制取氢气4g,问与足量稀硫酸反应的锌是多少克?
解:设需锌的质量为x
Zn+H2SO4=ZnSO4+H2↑
65 2
x 4g
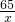 =
=
x=130g
答:需锌130g与足量的硫酸反应.
分析:由锌与硫酸反应的化学方程式,可以确定反应中锌与放出氢气的质量关系,利用需制取氢气的质量可计算消耗锌的质量.
点评:此题为根据化学方程式的基础计算,解答时注意解题的规范:正确书写化学方程式、完整的计算过程及正确的计算结果.
Zn+H2SO4=ZnSO4+H2↑
65 2
x 4g
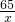 =
=
x=130g
答:需锌130g与足量的硫酸反应.
分析:由锌与硫酸反应的化学方程式,可以确定反应中锌与放出氢气的质量关系,利用需制取氢气的质量可计算消耗锌的质量.
点评:此题为根据化学方程式的基础计算,解答时注意解题的规范:正确书写化学方程式、完整的计算过程及正确的计算结果.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案
相关题目