题目内容
元素周期表是学习和研究化学的重要工具,它的内容十分丰富.下表是依据元素周期表画出的1-18号元素的原子结构示意图:

(1)1869年,科学家 发现了元素周期律和元素周期表.
(2)请画出17号元素原子结构示意图 .
(3)核电荷数为11的元素名称是 钠,在化学反应中,该元素的原子容易 (填“得”或“失”)电子;地壳中含量最多的金属元素的核电荷数是 ;
(4)对1-18号元素的原子结构示意图进行分析,可以发现许多规律,如第一周期元素的原子核外只有一个电子层.请再总结出其它规律,并写出其中一条: .
(5)一个水分子(H2O)共有 个原子核、 个质子.

(1)1869年,科学家
(2)请画出17号元素原子结构示意图
(3)核电荷数为11的元素名称是
(4)对1-18号元素的原子结构示意图进行分析,可以发现许多规律,如第一周期元素的原子核外只有一个电子层.请再总结出其它规律,并写出其中一条:
(5)一个水分子(H2O)共有
考点:元素周期表的特点及其应用,原子结构示意图与离子结构示意图
专题:化学用语和质量守恒定律
分析:(1)根据门捷列夫在化学科学上的主要成就回答.(2)根据17号元素原子的核外电子的排布情况作出结构示意图.(3)根据元素周期表中原子结构示意图的信息进行分析回答;(4)在元素周期表中,随原子序数的递增,原子结构中电子层数、最外层电子数发生规律性的变化,元素的种类(金属、非金属、稀有气体);(5)由图中1~18号元素原子最外层电子数与原子核电荷数的关系图可知:氢元素、氧元素的质子数.
解答:解:(1)1869年俄国的科学家门捷列夫发现了元素周期律,并首次编制了元素周期表,使化学学习和研究变得有规律可循.故填:门捷列夫;
(2)17号元素为氯元素,原子核内的质子数是17,原子结构示意图为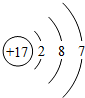 ;故填:
;故填: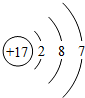 ;
;
(3)由11号元素的元素名称是钠元素,其原子结构示意图可知它的最外层有1个电子,故在化学反应中失去1个电子达到稳定结构,离子符号为Na+;地壳中含量最多的金属元素是铝元素,核电荷数为13;故填:钠;失;13;
(4)每一周期元素的原子的核外电子层数相同;每一周期元素原子的最外层电子数从左到右逐渐增加;每一纵列元素原子的最外层电子数相同等.故填:每一周期元素的原子的核外电子层数相同;
(5)根据“核内质子数=核外电子数=核电荷数”,由图中1~18号元素原子最外层电子数与原子核电荷数的关系图可知:氢元素、氧元素的质子数分别为:1、8;又因为1个水分子由2个氢原子和1个氧原子构成;故一个水分子共有3个原子核,1×2+8=10个质子;故填:3;10.
(2)17号元素为氯元素,原子核内的质子数是17,原子结构示意图为
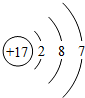 ;故填:
;故填: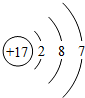 ;
;(3)由11号元素的元素名称是钠元素,其原子结构示意图可知它的最外层有1个电子,故在化学反应中失去1个电子达到稳定结构,离子符号为Na+;地壳中含量最多的金属元素是铝元素,核电荷数为13;故填:钠;失;13;
(4)每一周期元素的原子的核外电子层数相同;每一周期元素原子的最外层电子数从左到右逐渐增加;每一纵列元素原子的最外层电子数相同等.故填:每一周期元素的原子的核外电子层数相同;
(5)根据“核内质子数=核外电子数=核电荷数”,由图中1~18号元素原子最外层电子数与原子核电荷数的关系图可知:氢元素、氧元素的质子数分别为:1、8;又因为1个水分子由2个氢原子和1个氧原子构成;故一个水分子共有3个原子核,1×2+8=10个质子;故填:3;10.
点评:本题难度不大,考查学生灵活运用元素周期表中元素的信息、原子结构示意图及其意义进行分析解题的能力.

练习册系列答案
相关题目
下列变化中,分子的种类在变化前后一定发生改变的是( )
| A、动植物的呼吸作用 |
| B、水结成冰 |
| C、气球的爆炸 |
| D、矿石的粉碎 |
用量筒量取一定体积的液体,若俯视时读数为20mL,则实际量取的液体的体积为( )
| A、大于30mL |
| B、小于20mL |
| C、等于20mL |
| D、三种情况都有 |
下列关于原子构成的说法不正确的是( )
| A、原子中核外电子的质量很小 |
| B、原子不显电性,因为构成原子的粒子都不显电性 |
| C、原子核的体积仅为原子体积的几千亿分之一 |
| D、原子的质量主要集中在原子核上 |
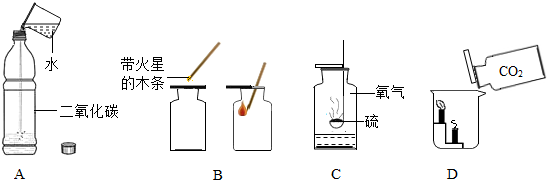
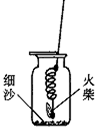 腾腾同学做细铁丝在氧气中的燃烧实验时,他把细铁丝绕成螺旋状,一端系在一根铁丝上,另食品包装袋内会充入
腾腾同学做细铁丝在氧气中的燃烧实验时,他把细铁丝绕成螺旋状,一端系在一根铁丝上,另食品包装袋内会充入