题目内容
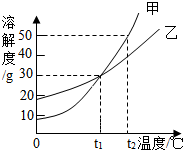 甲、乙两种物质的溶解度曲线如图所示.下列说法中正确的是( )
甲、乙两种物质的溶解度曲线如图所示.下列说法中正确的是( )| A、甲物质的溶解度大于乙物质的溶解度 |
| B、甲和乙的饱和溶液从t1℃升温到t2℃时都有晶体析出 |
| C、t1℃时,甲和乙各30g分别加入100g水中,充分溶解,均形成饱和溶液 |
| D、t2℃时,甲和乙的饱和溶液各100g其溶质的质量相等 |
考点:固体溶解度曲线及其作用,晶体和结晶的概念与现象
专题:溶液、浊液与溶解度
分析:A、根据溶解度的比较方法考虑;
B、对于饱和溶液升温而析出晶体,该物质的溶解度随温度升高而减小;
C、t1℃时,甲和乙的溶解度分析;
D、据溶解度的概念,溶液质量=溶质质量+溶剂质量解决此题.
B、对于饱和溶液升温而析出晶体,该物质的溶解度随温度升高而减小;
C、t1℃时,甲和乙的溶解度分析;
D、据溶解度的概念,溶液质量=溶质质量+溶剂质量解决此题.
解答:解:A、溶解度的比较必须有温度的限制,故A错误;
B、甲、乙两种物质的溶解度随温度升高而增大,故甲和乙的饱和溶液从t1℃升温到t2℃时都不会有晶体析出,故B错误;
C、由甲、乙两种物质的溶解度曲线知,t1℃时,甲和乙的溶解度都是30g,故t1℃时,甲和乙各30g分别加入100g水中,充分溶解,均形成饱和溶液,故C正确;
D、由甲、乙两种物质的溶解度曲线知,t2℃时,甲和乙的饱和溶液,甲的溶解度大于乙的溶解度,据溶液质量=溶质质量+溶剂质量,当溶液质量相同时,无法比较溶质的质量,故D错误.
故选C.
B、甲、乙两种物质的溶解度随温度升高而增大,故甲和乙的饱和溶液从t1℃升温到t2℃时都不会有晶体析出,故B错误;
C、由甲、乙两种物质的溶解度曲线知,t1℃时,甲和乙的溶解度都是30g,故t1℃时,甲和乙各30g分别加入100g水中,充分溶解,均形成饱和溶液,故C正确;
D、由甲、乙两种物质的溶解度曲线知,t2℃时,甲和乙的饱和溶液,甲的溶解度大于乙的溶解度,据溶液质量=溶质质量+溶剂质量,当溶液质量相同时,无法比较溶质的质量,故D错误.
故选C.
点评:主要考查了固体溶解度曲线的意义及固体溶解度和温度间的关系,并能利用所学知识来解决实际问题.

练习册系列答案
相关题目
下列关于仪器0刻度位置的叙述中正确的是( )
| A、在量筒上部 |
| B、在温度计的最下处 |
| C、在托盘天平标尺的正中 |
| D、在托盘天平的最左边 |
 向如图实验装置中通入气体X.若关闭活塞K,澄清石灰水变浑浊;打开活塞K,澄清石灰水始终不变浑浊.则气体X和洗气瓶内溶液Y分别可能是( )
向如图实验装置中通入气体X.若关闭活塞K,澄清石灰水变浑浊;打开活塞K,澄清石灰水始终不变浑浊.则气体X和洗气瓶内溶液Y分别可能是( )| A | B | C | D | |
| X | CO2 | HCl | CO2 | HCl |
| Y(足量) | NaOH溶液 | AgNO3溶液 | 浓硫酸 | Na2CO3溶液 |
| A、A | B、B | C、C | D、D |
下列化学用语书写不正确的是( )
| A、氯化铁 FeCl3 | ||
B、硫离子结构示意图 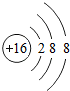 | ||
C、氨气(NH3)中氮元素的化合价:
| ||
| D、亚铁离子 Fe2+ |
 根据如图的信息判断,下列说法正确的是( )
根据如图的信息判断,下列说法正确的是( )| A、硫属于金属元素 |
| B、硫的相对原子质量为32.07g |
| C、硫原子的核电荷数为16 |
| D、在化学反应中,硫元素最高正化合价为+6价,最低化合价为-1价 |
除去下列物质中混有的少量杂质(括号内为杂质),所用试剂和方法中,不正确的是( )
| A、N2中的(O2):红热的木炭 |
| B、NaCl溶液中的(Na2CO3):加入稀盐酸 |
| C、FeCl2溶液中的(CuCl2):加入过量铁粉,过滤 |
| D、铜粉中的(铁):加入过量稀硫酸,过滤 |
下列反应属于复分解反应的是( )
| A、锌片投入稀硫酸中 |
| B、一氧化碳与氧化铜在加热条件下反应 |
| C、纯碱与盐酸 |
| D、在过氧化氢溶液中加入二氧化锰 |