题目内容
已知:A、B为常见的非金属单质且均为气体;甲、乙为金属单质,乙在I的浓溶液中发生钝化;C、H、J的溶液均呈碱性。各物质间的转化关系如下(部分生成物未给出,且未注明反应条件):

(1)写出反应②的化学方程式 。
(2)反应④中每消耗1 mol G,转移电子的物质的量为 。
(3)反应⑥的离子方程式是 。
(4)实验室中保存I的方法是 。
A、B为常见的非金属单质且均为气体,A、B反应的产物能连续两次与O2反应,C必为NH3,D为NO,G为NO2。以此为突破口,结合其余信息可推出,A、B、E、H、J、I、甲、乙分别为H2、N2、H2O、NaOH、NaAlO2、HNO3、Na、Al。
答案:(1)4NH3+5O2 4NO+6H2O(“高温”也可写成“△”)
4NO+6H2O(“高温”也可写成“△”)
(2)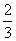 mol
mol
(3)2Al+2H2O+2OH-====2Al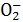 +3H2↑
+3H2↑
(4)保存在棕色试剂瓶中,放在阴凉处

下表是氯化钠和硝酸钾在不同温度时的溶解度,根据此表回答:
| 温度/℃ | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | NaCl | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
| KNO3 | 31.6 | 45.8 | 63.9 | 85.5 | 110 |
(1)60℃时,氯化钠的溶解度为____________g。
(2) 在30℃时,100 g水中加入50 g硝酸钾,充分搅拌后得到的溶液质量为____________g。
在30℃时,100 g水中加入50 g硝酸钾,充分搅拌后得到的溶液质量为____________g。
(3)欲从海水中获得氯化钠晶体,应采取________________________________
的方法。
(4)由表中数据分析可知,硝酸钾和氯化钠在某一温度时具有相同的溶解度x,则x的取值范围是_________________________________________。
如图A是某元素在元素周期表中的相关信息,B是其原子结构示意图,有关该元素及其原子结构的下列说法中,错误的是( )
| 13 Al 铝 26.98 |
|
| A | B |
A.该元素是原子序数为13
B.该原子在反应中容易失去3个电子
C.该元素属于金属元素
D.该元素的相对原子质量为26.98g
某有机物R和氧气置于完全封闭的容器中引燃,充分反应后,生成二氧化碳和水。实验测得反应前后物质质量如下表:
| R | O2 | CO2 | H2O | |
| 反应前质量(g) | 51 | 96 | 0 | 0 |
| 反应后质量(g) | x | 0 | 88 | 54 |
下列说法中不正确的是( )
A .x的值为5
.x的值为5  B.R物质中只含有碳、氢元素
B.R物质中只含有碳、氢元素
C.R物质中 碳氢元素的质量比为4∶1 D.反应生成的二氧化碳和水的分子个数比为2∶3
碳氢元素的质量比为4∶1 D.反应生成的二氧化碳和水的分子个数比为2∶3




 ?
?