题目内容
在化学反应中,物质所含元素的化合价发生变化的反应就是氧化还原反应.例如:2H2+Cl2 2HCl,反应前后H、Cl的化合价发生了变化,该反应是氧化还原反应.
2HCl,反应前后H、Cl的化合价发生了变化,该反应是氧化还原反应.(1)根据元素化合价发生变化的分析,下列反应属于氧化还原反应的是______;
①3Fe+2O2
 Fe3O4 ②H2O+CO2═H2CO3 ③NaOH+HCl═NaCl+H2O
Fe3O4 ②H2O+CO2═H2CO3 ③NaOH+HCl═NaCl+H2O④H2+CuO
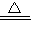 Cu+H2O ⑤2KMnO4
Cu+H2O ⑤2KMnO4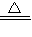 K2MnO4+MnO2+O2↑ ⑥CaCO3
K2MnO4+MnO2+O2↑ ⑥CaCO3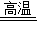 CaO+CO2↑
CaO+CO2↑(2)含有高价态元素的化合物,通常具有氧化性.如:将铜片放入氯化铁溶液中,氯化铁能将单质铜氧化成氯化铜,自身还原成氯化亚铁.该反应的化学方程式为
______.
【答案】分析:利用氧化还原反应的判定方法,以及书写化学反应方程式的方法来解答此题.
解答:解:(1)由题意可知,元素化合价发生变化就是发生了氧化还原反应.
①中,铁元素化合价由0变成了+2和+3,氧元素化合价由0变成了-2,所以为氧化还原反应;
④中,氢元素化合价由0变成了+1,铜元素化合价由+2变成了0,所以为氧化还原反应;
⑤中,锰元素化合价由+7变成了+6和+4,氧元素化合价由-2变成了0,所以为氧化还原反应;
②③⑥中各元素化合价没有发生变化,所以不是氧化还原反应.
(2)Fe3+可以把Cu氧化为Cu2+,自身被还原为Fe2+,所以将铜片放入氯化铁溶液中,反应的化学方程式为2FeCl3+Cu═2FeCl2+CuCl2
综上,答案为:①④⑤; 2FeCl3+Cu═2FeCl2+CuCl2
点评:此题考查了氧化还原反应的判定方法,以及书写化学反应方程式的方法,锻炼了学生分析问题解决问题的能力.
解答:解:(1)由题意可知,元素化合价发生变化就是发生了氧化还原反应.
①中,铁元素化合价由0变成了+2和+3,氧元素化合价由0变成了-2,所以为氧化还原反应;
④中,氢元素化合价由0变成了+1,铜元素化合价由+2变成了0,所以为氧化还原反应;
⑤中,锰元素化合价由+7变成了+6和+4,氧元素化合价由-2变成了0,所以为氧化还原反应;
②③⑥中各元素化合价没有发生变化,所以不是氧化还原反应.
(2)Fe3+可以把Cu氧化为Cu2+,自身被还原为Fe2+,所以将铜片放入氯化铁溶液中,反应的化学方程式为2FeCl3+Cu═2FeCl2+CuCl2
综上,答案为:①④⑤; 2FeCl3+Cu═2FeCl2+CuCl2
点评:此题考查了氧化还原反应的判定方法,以及书写化学反应方程式的方法,锻炼了学生分析问题解决问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
在化学反应中,物质所含元素的化合价发生变化的反应就是氧化还原反应.如:反应前后,钠元素、氯元素的化合价发生了变化,该反应是氧化还原反应.请你仔细阅读表格的内容,回答问题.
(1)请根据物质所含元素的化合价是否发生改变进行分析,表格内列出的化学方程式中属于氧化还原反应的是 (填序号).
(2)根据以下要求,写出有碳元素参加反应的化学方程式各一个:
分解反应: ;
置换反应: ;
化合反应: .
| 序号 | 化学方程式 | 属于的基本反应类型 | ||||
| 1 | Fe+S
|
Combination reaction | ||||
| 2 | Cu(OH)2
|
Deconpostition reaction | ||||
| 3 | H2+CuO
|
Displacenent reaction | ||||
| 4 | HCl+AgNO3=AgCl↓+HNO3 | Double deconposition reaction |
(2)根据以下要求,写出有碳元素参加反应的化学方程式各一个:
分解反应:
置换反应:
化合反应: