题目内容
8.一种含有铁和氧化铁的混合物与16.8g一氧化碳气体恰好完全反应.其中的氧化铁全部彼一氧化碳还原,最终所得固体质量为30.4g,则原混合物的质量为40g.分析 方法一:由于一氧化碳完全反应,所以可以根据一氧化碳求算生成的铁和消耗的氧化铁,进而求算出原混合物.
方法二:根据一氧化碳反应引起的固体质量差量,直接求算原混合物的总质量.
解答 解:
方法一:
设16.8g一氧化碳消耗的氧化铁的质量为x,生成的铁的质量为y.
Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
160 84 112
x 16.8g y
$\frac{160}{x}$=$\frac{84}{16.8g}$=$\frac{112}{y}$
x=32g
y=22.4g
则反应后对应的原混合物中的铁的质量为30.4g-22.4g=8g
则原混合物的质量为8g+32g=40g.
方法二:
原混合物的质量为x
Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 固体质量减少
160 84 112 48
16.8g x-30.4g
$\frac{84}{16.8g}$=$\frac{48}{x-30.4g}$
x=40g
故填:40.
点评 根据相关数据计算需要求算的物质,在数据选择时要结合变化的本质进行分析.本次提供的两种解法建议要认真思考,尤其是方法二作为差量法,这个解题思路很常用.

练习册系列答案
 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案
相关题目
18.如图为元素周期表的一部分(X元素信息不全).下列说法正确的是( )
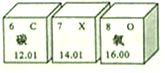

| A. | 氧的化学性质不活泼 | B. | X表示N2 | ||
| C. | 碳原子的质子数是6 | D. | 三种元素原子的核外电子数相同 |
3.如图的比例模型表示的是某反应的微观示意图●+○○$\stackrel{点燃}{→}$○●○(●表示碳原子,○表示氧原子).下列说法错误的是( )
| A. | 此反应为C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2 | B. | 此反应吸收热量 | ||
| C. | 此反应前后原子种类不变 | D. | 此反应属于化合反应 |
12.下列物质属于碱的是( )
| A. | Cu(OH)2CO3 | B. | H2SO4 | C. | NH3•H2O | D. | K2SO4 |
10.物质的下列性质中,属于物理性质的是( )
| A. | 氧气可以支持燃烧 | |
| B. | 活性炭可以吸附水中的颜色,异味 | |
| C. | CO2能使澄清石灰水变浑浊 | |
| D. | 常温下稀有气体的化学性质比较稳定 |
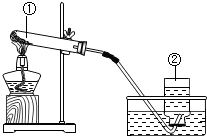 成了浅紫红色,你认为产生该现象的原因可能是试管口未塞一团棉花.
成了浅紫红色,你认为产生该现象的原因可能是试管口未塞一团棉花.