题目内容
4.世界卫生组织把铝列为食品污染源之一,每人每日摄入铝元素的量应控制在4mg以下.检査发现在1000g某种米面食品中加入了明矾2.37g[明矾的化学式为 KAl(SO4)2•12H2O,相对分子质量为474].请回答下列问题:(1)明矾由5种元素组成;明矾中含有硫酸根离子,该离子的符号为SO42-.
(2)明矾中铝、氧、氢元素的质是比为27:320:24.
(3)如果某人一天吃了 100g上述米面食品,摄入铝元素的质量为13.5mg.
分析 (1)根据明矾的化学式分析,
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(3)已知明矾中铝元素的质量分数,只要计算出100g面食品中明矾的质量,再根据明矾中铝元素的质量分数即可求出铝元素的质量即可.
解答 解:(1)明矾的化学式为 KAl(SO4)2•12H2O,可知明矾中含有 K、Al、S、O、H五种元素,硫酸根离子的符号为:SO42-;
(2)明矾中铝元素、氧元素、氢元素的质量比为:27:(16×20):(1×24)=27:320:24,
(3)100g上述面食品中铝的量=$\frac{2.37g}{1000g}$×100g×$\frac{27}{474}$×100%=0.0135g=13.5mg,
故答案为:(1)5;SO42-;
(2)27:320:24;
(3)13.5.
点评 本题属于根据化学式的相关基本计算,在平时做题中要注意,属于基础知识考查题.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.关于CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2,下列说法正确的是( )
| A. | 该反应是置换反应 | |
| B. | 反应前后碳元素的化合价由+2变为+4 | |
| C. | 反应中CO表现出氧化性 | |
| D. | 反应中CO的活动性比Cu强 |
19. 20℃时,将不同质量的NaCl晶体分别加入到100g水中,充分溶解后所得溶液的质量与加入氯化钠晶体质量的对应关系如下表:
20℃时,将不同质量的NaCl晶体分别加入到100g水中,充分溶解后所得溶液的质量与加入氯化钠晶体质量的对应关系如下表:
请回答下列问题:
(1)C组溶液中属于不饱和溶液(选填“饱和”或“不饱和”).
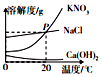
(2)KNO3、NaCl、Ca(OH)2三种物质的溶解度曲线如图所示. 则P点纵坐标的值为36.
(3)根据图象分析:饱和硝酸钾溶液中混有少量氯化钠,为提纯硝酸钾可采用的方法是降温结晶;室温时.向饱和石灰水中加入少量生石灰,并恢复至室温,此时溶液中溶质的质量<(选填“>”“<”或“=”)原溶液中溶质的质量.
 20℃时,将不同质量的NaCl晶体分别加入到100g水中,充分溶解后所得溶液的质量与加入氯化钠晶体质量的对应关系如下表:
20℃时,将不同质量的NaCl晶体分别加入到100g水中,充分溶解后所得溶液的质量与加入氯化钠晶体质量的对应关系如下表:| 组别 | A | B | C | D | E |
| NaCl晶体的质量/g | 5 | 15 | 20 | 30 | 40 |
| 所得溶液的质量/g | 105 | 115 | x | 130 | 136 |
(1)C组溶液中属于不饱和溶液(选填“饱和”或“不饱和”).
(2)KNO3、NaCl、Ca(OH)2三种物质的溶解度曲线如图所示. 则P点纵坐标的值为36.
(3)根据图象分析:饱和硝酸钾溶液中混有少量氯化钠,为提纯硝酸钾可采用的方法是降温结晶;室温时.向饱和石灰水中加入少量生石灰,并恢复至室温,此时溶液中溶质的质量<(选填“>”“<”或“=”)原溶液中溶质的质量.
9.青篙素(化学式为C15H22O5)是治疗疟疾的特效药.关于青篙素的说法正确的是( )
| A. | 一个青篙素分子含有11个氢分子 | |
| B. | 28.2g青篙素中含碳元素的质量为18g | |
| C. | 不属于有机物 | |
| D. | C、H、O三种元素的质量比为15:22:5 |
13.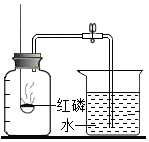 用如图所示装置测定空气中氧气的含量.不会使实验结果产生明显误差的是( )
用如图所示装置测定空气中氧气的含量.不会使实验结果产生明显误差的是( )
 用如图所示装置测定空气中氧气的含量.不会使实验结果产生明显误差的是( )
用如图所示装置测定空气中氧气的含量.不会使实验结果产生明显误差的是( )| A. | 点燃红磷前就打开止水夹 | |
| B. | 用木炭代替红磷进行实验 | |
| C. | 未等温度恢复到室温就进行测量 | |
| D. | 不打开橡胶塞,利用激光笔点燃红磷 |
14.中国著名药学家屠呦呦作为抗疟新药青嵩素(C15H22O5)的第一发明人获得了诺贝尔生理学或医学奖.下列有关青嵩素(C15H22O5)说法不正确的是( )
| A. | 青嵩素属于有机物 | |
| B. | 青嵩素中氢元素的质量分数最小 | |
| C. | 青嵩素的相对分子质量为282 | |
| D. | 青嵩素中C、H、O三种元素的质量比是15:22:5 |