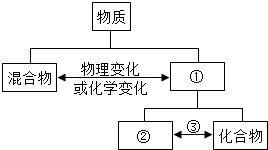
题目内容
海边盛产贝壳,其主要成分为CaCO3,以贝壳和纯碱为原料,生产烧碱的简要工艺流程下:
请回答下列问题:
(1)A的化学式是 .
(2)写出步骤①发生反应的化学方程式 .
(3)写出步骤②发生反应的化学方程式 .
(4)在工业上,熟石灰可用于生产烧碱.在农业上,它的一种用途是 .

请回答下列问题:
(1)A的化学式是
(2)写出步骤①发生反应的化学方程式
(3)写出步骤②发生反应的化学方程式
(4)在工业上,熟石灰可用于生产烧碱.在农业上,它的一种用途是
考点:物质的相互转化和制备,碳酸钙、生石灰、熟石灰之间的转化,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:物质的制备
分析:根据贝壳的主要成分为CaCO3,碳酸钙高温分解会生成氧化钙和二氧化碳,氧化钙和水反应会生成氢氧化钙,氢氧化钙俗称熟石灰,氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠等知识进行分析.
解答:解:(1)贝壳的主要成分为CaCO3,碳酸钙在高温条件下生成氧化钙和二氧化碳,所以A为氧化钙,化学式为CaO;
(2)步骤①发生的反应是碳酸钙在高温条件下生成氧化钙和二氧化碳,化学方程式为:CaCO3
CaO+CO2↑;
步骤②发生的反应是氧化钙和水反应生成氢氧化钙,化学方程式为:CaO+H2O=Ca(OH)2;
(3)氢氧化钙可以和酸发生中和反应,在农业上,可以用来改良酸性土壤.
故答案为:(1)CaO;
(2)CaCO3
CaO+CO2↑;CaO+H2O=Ca(OH)2;
(3)改良酸性土壤.
(2)步骤①发生的反应是碳酸钙在高温条件下生成氧化钙和二氧化碳,化学方程式为:CaCO3
| ||
步骤②发生的反应是氧化钙和水反应生成氢氧化钙,化学方程式为:CaO+H2O=Ca(OH)2;
(3)氢氧化钙可以和酸发生中和反应,在农业上,可以用来改良酸性土壤.
故答案为:(1)CaO;
(2)CaCO3
| ||
(3)改良酸性土壤.
点评:掌握碳酸钙、氧化钙、氢氧化钙之间的转化关系是正确解答本题的关键.

练习册系列答案
相关题目
如图是碳和碳的化合物的转化关系:
C
CO2→H2CO3
CaCO3
CO2
其各步转化的基本反应类型从左到右依次是( )
C
| CuO |
| Ca(OH)2 |
| 高温 |
其各步转化的基本反应类型从左到右依次是( )
| A、化合、分解、置换、复分解 |
| B、置换、化合、复分解、分解 |
| C、复分解、化合、分解、置换 |
| D、分解、置换、化合、复分解 |
有关酸碱中和反应说法正确的是( )
| A、蒸馒头时,在发酵的面团中加入一定量的纯碱,既能除去面团发酵过程中产生的酸,又能使馒头松软,这个反应属于中和反应 |
| B、中和反应都需要加入酚酞试液来判断反应的发生 |
| C、在中和反应中,发生反应的粒子是H+和OH- |
| D、向含有少量酚酞的氢氧化钠溶液中滴入稀盐酸,溶液变成了无色,说明二者恰好完全反应 |
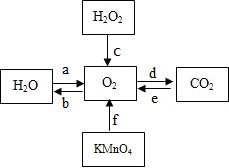 按要求完成下列各题:
按要求完成下列各题: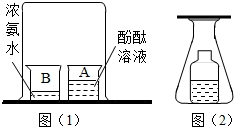 如图(1)和图(2)是两个设计证明分子运动的实验.在图(2)的锥形瓶中的小瓶里装着浓氨水,锥形瓶口用一张滤纸盖住,滤纸刚刚用酚酞溶液浸过.
如图(1)和图(2)是两个设计证明分子运动的实验.在图(2)的锥形瓶中的小瓶里装着浓氨水,锥形瓶口用一张滤纸盖住,滤纸刚刚用酚酞溶液浸过.