题目内容
13.根据所学知识并结合图1所示装置回答下列问题.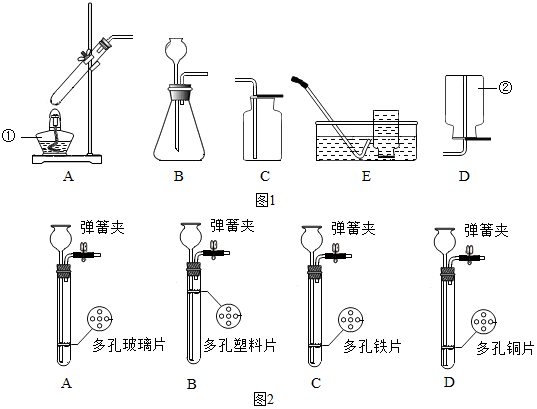
(1)图中标有①、②的仪器名称:①酒精灯,②集气瓶.
(2)用装置B制取气体时,若要能适当控制反应速率,则要进行的改进是将长颈漏斗换成分液漏斗.
(3)用高锰酸钾制取氧气的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,若选择A和C装置制取并收集氧气.则要对A装置进行的改进是试管口略向下倾斜,并在管口放一团棉花,调整试管高度.做铁丝在氧气中燃烧的实验时,收集氧气最好用E装置(填装置序号).
(4)如表是三种气体的密度(在0℃、101kPa条件下测定)和溶解程度.实验室要收集二氧化硫气体,可选用的装置是:C.
| 气体 性质 | 氢气 | 二氧化碳 | 二氧化硫 |
| 密度(g•L-1) | 0.08987 | 1.975 | 2.716 |
| 溶解程度 | 极难溶于水 | 能溶于水 | 易溶于水 |
分析 制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.
解答 解:(1)酒精灯是常用的加热仪器,集气瓶是常用收集气体的仪器.故答案为:①酒精灯、②集气瓶
(2)分液漏斗有控制反应速率的作用,长颈漏斗则不行,故答案为:将长颈漏斗换成分液漏斗
(3)高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,要注意配平.为防止药品中水分在加热时变成水蒸气在管口冷凝倒流,致使试管破裂要让试管口略向下倾斜;为防止高锰酸钾粉末进入导管,要并在管口放一团棉花为了方便加热,要调整试管高度.为防止铁的熔化物温度过高而炸裂集气瓶,要在集气瓶中留水,使用排水法收集氧气方便在集气瓶中留水.故答案为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$ K2MnO4+MnO2+O2↑;试管口略向下倾斜,并在管口放一团棉花,调整试管高度(写两点).E
(4)由表可知,二氧化硫易溶于水而且密度比空气大,故使用向上排空气法收集.故答案为:C
(5)启普发生器的隔离装置必须不能和反应物发生反应,图中只有铜片是不与盐酸发生反应的.长颈漏斗能用于添加液体.关闭弹簧夹,试管内气压增大,液面下降,使得盐酸与碳酸钙分离而停止反应.故答案为:D、长颈漏斗、关闭弹簧夹
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案| A. | 冬天室内用煤炉取暖要严防煤气中毒 | |
| B. | 汽车油箱着火,可以用水浇灭 | |
| C. | 发现厨房天然气泄露,打开抽油烟机排气 | |
| D. | 室内起火,迅速打开所有门窗通风 |
 核安全是2016国际外交的主题之一.核电站中核燃料铀或钚在中子的撞击下,原子核发生分裂,产生氙、锶等粒子和射线,同时释放大量的能量.锶元素在元素周期表中的信息和粒子结构示意图如图所示.以下表述中正确的是( )
核安全是2016国际外交的主题之一.核电站中核燃料铀或钚在中子的撞击下,原子核发生分裂,产生氙、锶等粒子和射线,同时释放大量的能量.锶元素在元素周期表中的信息和粒子结构示意图如图所示.以下表述中正确的是( )| A. | 锶原子的原子质量是87.62 | B. | 图3所表示粒子的化学符号是Sr | ||
| C. | 反应中锶元素易失去电子 | D. | 锶原子的中子数为38 |
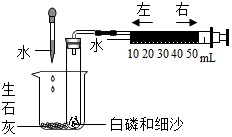 某化学小组利用如图所示实验装置测定空气中氧气的含量(部分固定装置已略去).关于该实验有下列说法:①向烧杯中加水是为了提高烧杯内的温度;②白磷燃烧会放出大量的白雾;③白磷的量不足,会使测定的结果偏大;④实验中可观察到,注射器的活塞先向右移动,后向左移动;⑤若试管内净容积为50mL,反应后冷却至室温,活塞停止在40mL附近.其中正确的是( )
某化学小组利用如图所示实验装置测定空气中氧气的含量(部分固定装置已略去).关于该实验有下列说法:①向烧杯中加水是为了提高烧杯内的温度;②白磷燃烧会放出大量的白雾;③白磷的量不足,会使测定的结果偏大;④实验中可观察到,注射器的活塞先向右移动,后向左移动;⑤若试管内净容积为50mL,反应后冷却至室温,活塞停止在40mL附近.其中正确的是( )| A. | ①②③ | B. | ②③⑤ | C. | ③④⑤ | D. | ①④⑤ |
| A. | 煅烧石灰石 | B. | 一氧化碳还原氧化铜 | ||
| C. | 木炭燃烧 | D. | 干冰升华 |
| A. | 氧气 | B. | 氢气 | C. | 一氧化碳 | D. | 二氧化碳 |

