题目内容
20.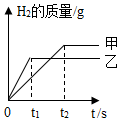 将等质量锌粉和铁粉,分别放入相同的足量稀盐酸中,反应后生成氢气质量与反应时间的关系如图所示,据图回答:
将等质量锌粉和铁粉,分别放入相同的足量稀盐酸中,反应后生成氢气质量与反应时间的关系如图所示,据图回答:(1)金属甲是铁,判断的理由是锌的金属活动性比铁强,甲的反应速率小;
(2)从图中还可以获得的信息有铁生成的氢气多.
分析 根据金属活动性顺序可知,金属越活泼,与稀盐酸反应的速率越快进行分析.
解答 解:金属活动性顺序可知,金属越活泼,与稀盐酸反应的速率越快,金属的相对原子质量越大,等质量的金属与酸反应时,生成的氢气质量越小,所以
(1)金属甲是铁,判断的理由是:锌的金属活动性比铁强,甲的反应速率小;
(2)从图中还可以获得的信息有:铁生成的氢气多.
故答案为:(1)铁,锌的金属活动性比铁强,甲的反应速率小;
(2)铁生成的氢气多.
点评 由图中信息可知,反应需要的时间越短,说明反应速率越快,反应需要的时间越长,说明反应速率越慢,要注意理解.

练习册系列答案
 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南大学出版社系列答案
同步练习西南大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案
相关题目
10.二氧化碳是造成温室效应的主要气体之一,下列说法错误的是( )
| A. | 越来越多煤、石油、天然气等物质的燃烧使二氧化碳增加 | |
| B. | 人口增长太快,森林被大量砍伐,导致自然界消耗二氧化碳能力降低 | |
| C. | 实验室加热碳酸氢铵分解是二氧化碳含量增加的主要原因 | |
| D. | 工业发展排放的二氧化碳等温室气体增加 |
11.下列实验操作的图示正确的是( )
| A. |  放块状固体 | B. |  读液体体积 | ||
| C. |  向试管中倾倒液体 | D. |  给液体加热 |
8.下列公共标志与消防安全无关的是( )


| A. | ①② | B. | ②③ | C. | ③④ | D. | ③④⑤ |
5.下列有关质量守恒定律的理解,正确的是( )
| A. | 5g铁和5g铜混合,物质的总质量为10g,遵守质量守恒定律 | |
| B. | 化学反应前后分子的总数一定不会发生改变 | |
| C. | 5g硫和5g氧气完全反应,生成物质量为10g,遵守质量守恒定律 | |
| D. | 镁条燃烧后质量增加,未遵守质量守恒定律 |
9.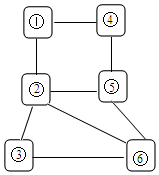 如图中连线两端的物质在通常情况下可以相互反应,下列四组选项中,符合该图要求的是( )
如图中连线两端的物质在通常情况下可以相互反应,下列四组选项中,符合该图要求的是( )
 如图中连线两端的物质在通常情况下可以相互反应,下列四组选项中,符合该图要求的是( )
如图中连线两端的物质在通常情况下可以相互反应,下列四组选项中,符合该图要求的是( )| ① | ② | ③ | ④ | ⑤ | ⑥ | |
| A | CO2 | NaOH | HCl | Ca(OH)2 | CuCl2 | Fe |
| B | CaO | HCl | Fe | H2SO4 | Na2CO3 | Ca(OH)2 |
| C | Fe | H2SO4 | BaCl2 | Cu(NO3)2 | Ca(OH)2 | Na2CO3 |
| D | Zn | HCl | CaCO3 | CuSO4 | NaOH | FeCl3 |
| A. | A | B. | B | C. | C | D. | D |