题目内容
锌与稀硫酸反应生成硫酸锌和氢气.实验室用13g锌和足量的稀硫酸反应,可生成多少克氢气?同时可以得到硫酸锌多少克?
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:根据锌的质量和反应的化学方程式可以计算生成氢气和硫酸锌的质量.
解答:解:设生成氢气、硫酸锌的质量分别是x、y,
Zn+H2SO4═ZnSO4+H2↑,
65 161 2
13g y x
=
=
,
x=0.4g,y=32.2g,
答:用13g锌和足量的稀硫酸反应,生成氢气和硫酸锌的质量分别是0.4g和32.2g.
Zn+H2SO4═ZnSO4+H2↑,
65 161 2
13g y x
| 65 |
| 13g |
| 161 |
| y |
| 2 |
| x |
x=0.4g,y=32.2g,
答:用13g锌和足量的稀硫酸反应,生成氢气和硫酸锌的质量分别是0.4g和32.2g.
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案
相关题目
如图所示:2个甲分子反应生成1个丙分子和3个乙分子,下列判断不正确的是( )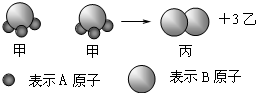

| A、丙分子中元素的化合价为零 |
| B、参加反应的甲物质属于化合物 |
| C、该化学反应中原子的种类发生了改变 |
| D、根据质量守恒定律可推知,1个乙分子中含有2个A原子 |
下列说法正确的是( )
| A、爆炸都是由燃烧引发的 |
| B、工业上用分离液态空气的方法制氧气属于化学变化 |
| C、铁的生锈属于缓慢氧化 |
| D、俯视或仰视读取量筒内液体体积时,不会影响实验结果的精确性 |

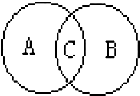 如果A、B两圆分别表示化合反应和氧化反应,C表示A、B反应的集合; 请你根据两圆关系来回答下列问题.
如果A、B两圆分别表示化合反应和氧化反应,C表示A、B反应的集合; 请你根据两圆关系来回答下列问题.