题目内容
20.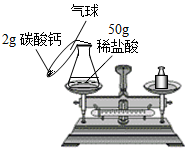 小李用盐酸与碳酸钙粉末反应验证质量守恒定律,实验装置如图
小李用盐酸与碳酸钙粉末反应验证质量守恒定律,实验装置如图(1)根据实验目的,小李必须测量的数据是CD
A.锥形瓶质量
B.气球质量
C.反应前整个反应装置(包括里边的物质)质量
D.反应后整个反应装置(包括里边的物质)质量
(2)将反应装置放在天平左盘,使天平平衡后,再将碳酸钙粉末倒入锥形瓶中.反应结束后,气球鼓起,天平向右倾斜.小李按规范操作重新实验,得到相同结果.请你帮他分析原因气球膨胀,收到的浮力增大
(3)反应结束后,锥形瓶中无固体剩余,则生成气体质量0.88g,所得溶液中生成物的溶质质量分数(只需写出最终的计算表达式)$\frac{2.22g}{50g+2g-0.88g}$×100%.
分析 根据已有的知识进行分析,验证质量守恒定律,则需要测定反应前后物质的总质量,碳酸钙和稀盐酸反应能生成氯化钙、水和二氧化碳;根据化学方程式进行计算,根据碳酸钙的质量可以计算生成二氧化碳的质量和氯化钙的质量,据此解答.
解答 解:(1)验证质量守恒定律,则需要测定反应前后物质的总质量,故选CD;
(2)天平向右倾斜是因为气球膨胀,收到的浮力增大,故填:气球膨胀,收到的浮力增大.
(3)设生成二氧化碳的质量为x,生成的氯化钙的质量为y,
CaCO3+2HCl═CaCl2+H2O+CO2↑,
100 111 44
2g y x
则$\frac{100}{44}$=$\frac{2g}{x}$,解得x=0.88g,
$\frac{100}{111}$=$\frac{2g}{y}$,解得y=2.22g,所得溶液中生成物的溶质质量分数为$\frac{2.22g}{50g+2g-0.88g}$×100%
故答案为:0.88;$\frac{2.22g}{50g+2g-0.88g}$×100%.
点评 本题考查了质量守恒定律的实验探究,完成此题,可以依据探究过程中的注意事项进行.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
15.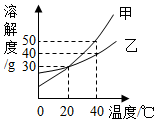 如图,是甲、乙两种固体物质的溶解度曲线,下列说法正确的是( )
如图,是甲、乙两种固体物质的溶解度曲线,下列说法正确的是( )
 如图,是甲、乙两种固体物质的溶解度曲线,下列说法正确的是( )
如图,是甲、乙两种固体物质的溶解度曲线,下列说法正确的是( )| A. | 20℃时,甲、乙两种固体物质的溶解度都是30 | |
| B. | 40℃时,甲的饱和溶液中溶质质量分数为50% | |
| C. | 40℃时,将50g乙物质全部溶于水中,恰好能得到150g乙的饱和溶液 | |
| D. | 将130g20℃甲的饱和溶液升温到40℃,最多还能溶解甲物质20g |
5.如图所示实验操作正确的是( )
| A. |  滴加液体 | B. |  闻气体气味 | C. |  熄灭酒精灯 | D. |  稀释浓硫酸 |
12.下列科学家与他的贡献对应不正确的是( )
| A. | 侯德榜---联合制碱法 | |
| B. | 门捷列夫---元素周期表 | |
| C. | 阿基米德---杠杆原理:F1l1=F2l2 | |
| D. | 欧姆---电流通过导体产生的热量:Q=I2Rt |
9.在一密闭容器内加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,反应前后各物质的质量变化见表.下列说法错误的是( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前物质的质量(g) | 8 | 32 | 5 | 4 |
| 反应前物质的质量(g) | 16 | X | 5 | 24 |
| A. | 该反应为分解反应 | |
| B. | 丙可能是该反应的催化剂 | |
| C. | 甲、丁两物质反应前后质量变化之比为2:5 | |
| D. | X值为28 |
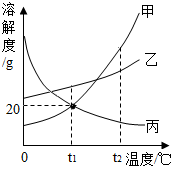 甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线如图所示.
甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线如图所示.