题目内容
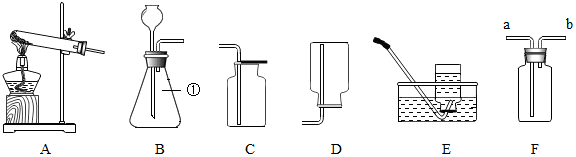
6.如图是一定条件下相关物质的转化关系,A、F是两种铁矿石,主成份是由2种相同的元素组成的不同的化合物,其中,A为红棕色固体.白色沉淀I是石灰石、大理石等矿石的主要成分,B、C、E均是初中常见的一种无色、无味的气体.
(1)写出下列物质的化学式:ICaCO3,FFe3O4.
(2)若G是一种气态单质,则X可能的化学式是H2SO4或HCl;若X是一种常见的蓝色溶液,则④的反应方程式是Fe+CuSO4=FeSO4+Cu.
(3)写出:①反应的化学方程式3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2、②反应的化学方程式2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2.
分析 氧化铁在高温条件下和一氧化碳反应生成铁和二氧化碳,铁在氧气中燃烧生成四氧化三铁;
铁和稀盐酸反应生成氯化亚铁和氢气,和稀硫酸反应生成硫酸亚铁和氢气,亚铁盐溶液是浅绿色溶液;
一氧化碳燃烧生成二氧化碳,二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,高温条件下碳酸钙分解生成氧化钙和二氧化碳.
解答 解:氧化铁在高温条件下和一氧化碳反应生成铁和二氧化碳,铁在氧气中燃烧生成四氧化三铁;
铁和稀盐酸反应生成氯化亚铁和氢气,和稀硫酸反应生成硫酸亚铁和氢气,亚铁盐溶液是浅绿色溶液;
一氧化碳燃烧生成二氧化碳,二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,高温条件下碳酸钙分解生成氧化钙和二氧化碳,因此A~I分别是氧化铁、一氧化碳、氧气、铁、二氧化碳、四氧化三铁、氢气、氯化亚铁或硫酸亚铁和碳酸钙;
(1)I是碳酸钙,化学式是CaCO3,F是四氧化三铁,化学式是Fe3O4.
故填:CaCO3;Fe3O4.
(2)若G是一种气态单质,则G是氢气,则X可能的化学式是H2SO4或HCl;
硫酸铜溶液是一种常见的蓝色溶液,则④的反应方程式是:Fe+CuSO4=FeSO4+Cu.
故填:H2SO4或HCl;Fe+CuSO4=FeSO4+Cu.
(3)①中氧化铁和一氧化碳反应生成铁和二氧化碳,反应的化学方程式为:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
②中一氧化碳燃烧生成二氧化碳,反应的化学方程式为:2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2.
故填:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

①通入澄清石灰水
②通入紫色石蕊试液
③闻气味
④通过灼热的氧化铜
⑤在密闭的容器中用活的昆虫试验,观察昆虫是否死亡
⑥点燃看能否燃烧.
| A. | ①② | B. | ③⑥ | C. | ③⑤ | D. | ①③ |
| A. | 菜刀用后洗净擦干 | |
| B. | 废旧电池随意丢弃 | |
| C. | 霉变大米洗净后继续食用,以免浪费 | |
| D. | 尽可能多吃含微量元素的保健品 |
| A. | 蒸发5 g水有固体溶质析出 | B. | 加入少许硝酸钾晶体不溶 | ||
| C. | 把溶液降温至 0℃有固体溶质析出 | D. | 上述三种方法都行 |
| A. | 氧气O2 | B. | 氯化亚铁FeCl2 | C. | 硫酸钠NaSO4 | D. | 氯化铵NH4Cl |
(2)氧气气由氧分子构成的(写出具体粒子名称,下同),铁由铁原子构成的,氯化钠由钠离子、氯离子构成的.
(3)有的物质由分子构成,还有的物质是由原子直接构成的,分子和原子的本质区别是在化学变化中分子能再分而原子不能再分.
(4)分子是由原子构成的.二氧化硫分子是由氧原子和硫原子构成的
(5)填写下表:
| 原子的种类 | 核电荷数 | 质子数 | 中子数 | 核外电子数 | 相对原子质量 |
| 铁 | 26 | 26 | 30 | 26 | 56 |
| 磷 | 15 | 15 | 16 | 15 | 31 |