题目内容
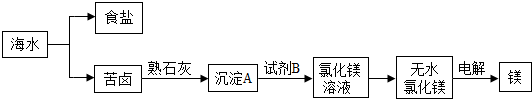
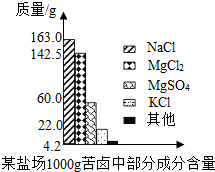
苦卤是海水提取食盐后的残液,其含有多种成分,在食品、化工等方面有重要应用.下图1是我国某盐场苦卤中各成分含量的柱型图.
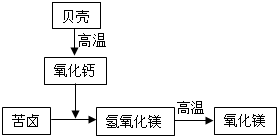
(1)该盐场以苦卤和贝壳为原料按图2所示过程生产轻质氧化镁.此生产过程中主要涉及了五个化学反应,其中没有出现过的反应类型是(______)
A.化合反应 B 分解反应 C 复分解反应 D 置换反应

(2)写出其中两个不同类型的化学反应.______ CaO+CO2↑
【答案】分析:(1)过程中涉及碳酸钙、氢氧化镁的高温分解,生石灰与水的化合,熟石灰与氯化镁、硫酸镁的复分解;
(2)生产过程所涉及的五个反应的化学方程式及反应类型为:分解反应:CaCO3 CaO+CO2↑和Mg(OH)2
CaO+CO2↑和Mg(OH)2 H2O+MgO;
H2O+MgO;
化合反应:CaO+H2O=Ca(OH)2;复分解反应:Ca(OH)2+MgCl2=Mg(OH)2↓+CaCl2和Ca(OH)2+MgSO4=Mg(OH)2↓+CaSO4;
(3)根据反应过程中元素质量不变,生成氧化镁中镁元素的质量与苦卤中镁元素质量相等;苦卤中镁元素质量为氯化镁中镁元素与硫酸镁中镁元素的质量和;根据这一等量关系,可利用1500g苦卤中氯化镁和硫酸镁的质量计算生成的氧化镁的质量.
解答:解:(1)以苦卤和贝壳为原料按图2所示过程生产轻质氧化镁过程经历了:碳酸钙的高温分解→生石灰与水的化合→熟石灰与氯化镁、硫酸镁的复分解→氢氧化镁的高温分解;因此,过程中没有涉及置换反应;
故答案为:D;
(2)生产过程中出现:
两个分解反应,分别为:CaCO3 CaO+CO2↑和Mg(OH)2
CaO+CO2↑和Mg(OH)2 H2O+MgO;
H2O+MgO;
一个化合反应,为:CaO+H2O=Ca(OH)2;
两个复分解反应,分别为:Ca(OH)2+MgCl2=Mg(OH)2↓+CaCl2和Ca(OH)2+MgSO4=Mg(OH)2↓+CaSO4;
因此其中两个不同类型的化学反应,可在三种类型的五个反应中选择进行组合,本题答案可有多种;
故答案为:CaCO3 CaO+CO2↑,CaO+H2O=Ca(OH)2[或Ca(OH)2+MgCl2=Mg(OH)2↓+CaCl2或Ca(OH)2+MgSO4=Mg(OH)2↓+CaSO4或
CaO+CO2↑,CaO+H2O=Ca(OH)2[或Ca(OH)2+MgCl2=Mg(OH)2↓+CaCl2或Ca(OH)2+MgSO4=Mg(OH)2↓+CaSO4或
Mg(OH)2 H2O+MgO]
H2O+MgO]
(3)设可生产氧化镁的质量为x,则:
142.5g× ×
× ×100%+80.0g×
×100%+80.0g× ×
× ×100%=x×
×100%=x× ×100%
×100%
解之得x=130g
答:能制得氧化镁130g.
点评:化学变化分为四种基本反应类型,反应特点可归纳为:化合反应,A+B=C;分解反应,C=A+B;置换反应,A+BC=AC+B;复分解反应,AB+CD=AD+CB.
(2)生产过程所涉及的五个反应的化学方程式及反应类型为:分解反应:CaCO3
 CaO+CO2↑和Mg(OH)2
CaO+CO2↑和Mg(OH)2 H2O+MgO;
H2O+MgO;化合反应:CaO+H2O=Ca(OH)2;复分解反应:Ca(OH)2+MgCl2=Mg(OH)2↓+CaCl2和Ca(OH)2+MgSO4=Mg(OH)2↓+CaSO4;
(3)根据反应过程中元素质量不变,生成氧化镁中镁元素的质量与苦卤中镁元素质量相等;苦卤中镁元素质量为氯化镁中镁元素与硫酸镁中镁元素的质量和;根据这一等量关系,可利用1500g苦卤中氯化镁和硫酸镁的质量计算生成的氧化镁的质量.
解答:解:(1)以苦卤和贝壳为原料按图2所示过程生产轻质氧化镁过程经历了:碳酸钙的高温分解→生石灰与水的化合→熟石灰与氯化镁、硫酸镁的复分解→氢氧化镁的高温分解;因此,过程中没有涉及置换反应;
故答案为:D;
(2)生产过程中出现:
两个分解反应,分别为:CaCO3
 CaO+CO2↑和Mg(OH)2
CaO+CO2↑和Mg(OH)2 H2O+MgO;
H2O+MgO;一个化合反应,为:CaO+H2O=Ca(OH)2;
两个复分解反应,分别为:Ca(OH)2+MgCl2=Mg(OH)2↓+CaCl2和Ca(OH)2+MgSO4=Mg(OH)2↓+CaSO4;
因此其中两个不同类型的化学反应,可在三种类型的五个反应中选择进行组合,本题答案可有多种;
故答案为:CaCO3
 CaO+CO2↑,CaO+H2O=Ca(OH)2[或Ca(OH)2+MgCl2=Mg(OH)2↓+CaCl2或Ca(OH)2+MgSO4=Mg(OH)2↓+CaSO4或
CaO+CO2↑,CaO+H2O=Ca(OH)2[或Ca(OH)2+MgCl2=Mg(OH)2↓+CaCl2或Ca(OH)2+MgSO4=Mg(OH)2↓+CaSO4或Mg(OH)2
 H2O+MgO]
H2O+MgO](3)设可生产氧化镁的质量为x,则:
142.5g×
 ×
× ×100%+80.0g×
×100%+80.0g× ×
× ×100%=x×
×100%=x× ×100%
×100%解之得x=130g
答:能制得氧化镁130g.
点评:化学变化分为四种基本反应类型,反应特点可归纳为:化合反应,A+B=C;分解反应,C=A+B;置换反应,A+BC=AC+B;复分解反应,AB+CD=AD+CB.

练习册系列答案
相关题目
 海洋约占地球表面积的71%,具有十分巨大的开发潜力.苦卤是海水提取食盐后的残液,利用苦卤可以制得金属镁等化工原料.下图是我市某盐场苦卤中部分成分含量柱形图.试计算:
海洋约占地球表面积的71%,具有十分巨大的开发潜力.苦卤是海水提取食盐后的残液,利用苦卤可以制得金属镁等化工原料.下图是我市某盐场苦卤中部分成分含量柱形图.试计算: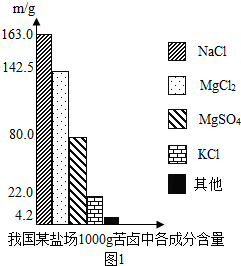
 海洋约占地球表面积的71%,具有十分巨大的开发潜力.苦卤是海水提取食盐后的残液,利用苦卤可以制得金属镁等化工原料.如图是某盐场苦卤中部分成分含量柱形图.试计算:
海洋约占地球表面积的71%,具有十分巨大的开发潜力.苦卤是海水提取食盐后的残液,利用苦卤可以制得金属镁等化工原料.如图是某盐场苦卤中部分成分含量柱形图.试计算: 地球资源是人类赖于生存的基础.今年4月22日“世界地球日”的主题是“珍惜地球资源、转变发展方式”.
地球资源是人类赖于生存的基础.今年4月22日“世界地球日”的主题是“珍惜地球资源、转变发展方式”.